
【题目】下列方法中,可以使0.10 mol·L-1 CH3COOH溶液中CH3COOH电离程度增大的是
A. 加入少量冰醋酸 B. 加水稀释
C. 加入少量氯化钠固体 D. 加入少量醋酸钠固体
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题:
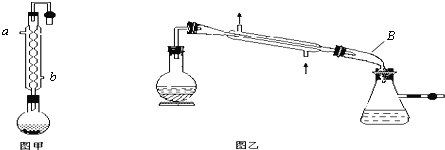
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入__________,目的是__________。
(2)反应中加入过量的乙醇,目的是__________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴
加乙酸边加热蒸馏。这样操作可以提高酯的产率,其原因是____________________。
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:

则试剂a是:____________,分离方法I是____________,分离方法II是____________,
试剂b是______________,分离方法III是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
汽车尾气净化的主要原理为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
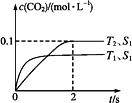
据此判断:
(1)该反应的ΔH____(填“>”或“<”)0。
(2)在T2温度下,0~2 s内的平均反应速率v(N2)=____。
(3)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。___________________
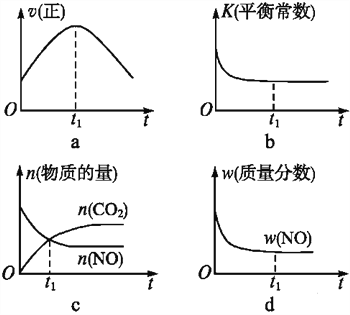
(4)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定容积的密闭容器中发生下列反应∶2HI(g)![]() H2(g)+I2(g)。若HI的浓度由0.1 mol L-1 降到0.07 mol L-1时需要15s,则HI的浓度由0.07 mol L-1降到0.05 mol L-1时,所需时间为
H2(g)+I2(g)。若HI的浓度由0.1 mol L-1 降到0.07 mol L-1时需要15s,则HI的浓度由0.07 mol L-1降到0.05 mol L-1时,所需时间为
A.等于15s B.等于10 s C.大于10s D.小于10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应的热化学方程式是
2NH3的能量变化如图所示,该反应的热化学方程式是

A.0.5N2(g)+1.5H2(g)![]() NH3(l)△H=(b+c﹣a)kJ/mol
NH3(l)△H=(b+c﹣a)kJ/mol
B.0.5N2(g)+1.5H2(g)![]() NH3(g)△H=(a+b)kJ/mol
NH3(g)△H=(a+b)kJ/mol
C.N2(g)+3H2(g)![]() 2NH3(l)△H=2(a﹣b﹣c)kJ/mol
2NH3(l)△H=2(a﹣b﹣c)kJ/mol
D.N2(g)+3H2(g)![]() 2NH3(g)△H=2(b﹣a)kJ/mol
2NH3(g)△H=2(b﹣a)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取少量乙酸乙酯的装置图,下列关于该实验的叙述中,不正确的是

A. 向a试管中先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸
B. 可将饱和碳酸钠溶液换成氢氧化钠溶液
C. 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
D. 实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质](15分)
“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O]![]() 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
(1)铁元素在元素周期表中的位置为 ,其价层电子排布图为 。
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为 。“摩尔盐”的分解产物中属于非极性分子的化合物是____。
(3)NH3的沸点比N2O的沸点 (填“高”或“低”),其主要原因是 。
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为_______ ____,与CN—互为等电子体的单质的分子式为___ _。HCN分子中σ键和π键的个数之比为 。
(5)FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为__________,若该晶胞边长为acm,则该晶胞密度为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+3B(g)![]() 2C(g)+D(g)在四种不同条件下的反应速率分别为:
2C(g)+D(g)在四种不同条件下的反应速率分别为:
①![]() (A)=0.5 mol·L—l·min—l ②
(A)=0.5 mol·L—l·min—l ②![]() (B)=0.6 mol·L—l·min—l
(B)=0.6 mol·L—l·min—l
③![]() (C)=0.35 mol·L—l·min—l ④
(C)=0.35 mol·L—l·min—l ④![]() (D)=0.4 mol·L—l·min—l
(D)=0.4 mol·L—l·min—l
则该反应在不同条件下反应速率最快的是( )
A. ① B. ② C. ③ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)CO是合成尿素、甲酸的原料。
(1)在100 kPa和T K下,由稳定单质生成1 mol化合物的焓变称为该物质在T K时的标准摩尔生成焓,用符号ΔHm0表示。已知石墨和CO的标准燃烧热分别为393.5 kJmol1和283.0 kJmol1,则CO(g)的ΔHm0= 。
(2)合成尿素的反应:2NH3(g) + CO(g) == CO(NH2)2(g) + H2(g) ΔH =81.0 kJmol1。
①T ℃时,在体积为2 L的恒容密闭容器中,将2 molNH3和1 mol CO混合发生反应,5 min时,NH3的转化率为80%。则0~5 min内的平均反应速率为v(CO)= 。
②已知:
温度/K | 398 | 498 | … |
平衡常数(K) | 126.5 | K1 | … |
则:K1 126.5(填“>”或“<”);其判断理由是 。
③若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示:

若图中c表示平衡体系中尿素的体积分数,则a表示 的转化率。
当![]() = 时,尿素含量最大;此时,对于该反应既能增大正反应速率又能使平衡正向移动的措施是 (写一种)。
= 时,尿素含量最大;此时,对于该反应既能增大正反应速率又能使平衡正向移动的措施是 (写一种)。
(3)通过人工光合作用可将CO转化成HCOOH。
①已知常温下,浓度均为0.1 molL1的HCOOH和HCOONa混合溶液pH =3.7,则HCOOH的电离常数Ka的值为 (已知lg2=0.3)。
②用电化学可消除HCOOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。Co3+氧化HCOOH的离子方程式为 ;忽略体积变化,电解前后Co2+的浓度将 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com