
| 实验步骤 | 实验现象 | 实验结论 |
ⅰ、取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中 | 气泡产生,澄清的石灰水变浑浊 | 证明含有碳酸根离子 |
| ⅱ、取第二份溶液,分别滴加稀盐酸和氯化钡 | 白色沉淀 | 证明含有硫酸根离子 |
| ⅲ、取第三份溶液加入过量BaCl2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有氯离子. |
| ⅳ、取第四份溶液进行焰色反应 | 透过蓝色钴玻璃火焰呈紫色 | 证明含有K+ |
分析 (1))①取草木灰加水溶解,用玻璃棒搅拌,加速溶解;②过滤,用玻璃棒引流;③蒸发滤液时用玻璃棒搅拌,加速蒸发;
(2)检验草木灰中的离子,焰色反应检验钾离子,加盐酸、氯化钡等可检验碳酸根离子;
(3)iii中引入氯离子,干扰实验;
(4)步骤ii生成的白色沉淀为硫酸钡,发生硫酸钾与氯化钡的反应.
解答 解:(1)①取草木灰加水溶解,用玻璃棒搅拌,加速溶解;②过滤,用玻璃棒引流;③蒸发滤液时用玻璃棒搅拌,加速蒸发,故答案为:①②③;
(2)检验草木灰中的离子,加盐酸有气泡产生,则含碳酸根离子;
取第二份溶液,先别滴加稀盐酸,后加氯化钡溶液,若生成白色沉淀,含硫酸根离子;
取第三份溶液加入过量BaCl2溶液,过滤,除去SO4-和CO32-,再滴加AgNO3溶液和稀硝酸,有白色沉淀生成,为AgCl;
取第四份溶液进行焰色反应,透过蓝色钴玻璃火焰呈紫色,则含钾离子,
故答案为:
| 实验步骤 | 实验现象 | 实验结论 |
i、取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中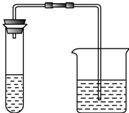 | 气泡产生,澄 清的石灰水变浑浊 | 证明含有碳酸根离子 |
| ⅱ、取第二份溶液,先别滴加稀盐酸,后加 氯化钡 | 白色沉淀 | 证明含有硫酸根离子 |
| ⅲ、取第三份溶液加入过量BaCl2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有氯离子 |
| iv、取第四份溶液进行焰色反应 | 透过蓝色钴玻璃 火焰呈紫色 | 证明含有K+ |
点评 本题考查物质的组成及物质的鉴别,为高频考点,把握实验基本操作及离子之间的反应为解答的关键,侧重物质性质及反应现象的考查,注意常见离子的检验,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和甲苯中都含有甲基,甲苯可以被酸性KMnO4溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响 | |
| B. | 苯和浓硝酸、浓硫酸混合物在100~110℃才能生成二硝基苯,而甲苯在100℃时即可生成三硝基甲苯,说明甲基对苯环产生了影响 | |
| C. | 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 | |
| D. | 除去苯中混入的少量甲苯可加入适量的酸性KMnO4溶液,充分反应后再加入足量的NaOH溶液,然后分液即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应的焓变与反应的途径有关 | |
| B. | 室温下,稀释0.1mol•L-1CH3COOH溶液,溶液的导电能力减弱 | |
| C. | 常温常压下,22.4L Cl2中含有的分子数为6.02×1023个 | |
| D. | 等质量的铜按a、b两种途径完全转化为Cu(NO3)2,途径a、b消耗的硝酸一样多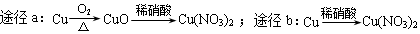 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | 在c(H+)=1×10-13mol•L-1的溶液中:Na+、Fe3+、Cl-、SO42-能大量共存 | |
| C. | 铜溶于FeCl3溶液中:Cu+Fe3+=Fe2++Cu2+ | |
| D. | 向溶液中加入BaCl2溶液后再加盐酸,有白色沉淀,说明该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
将1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体 1120 mL(标准状况),向反应后的溶液中加入1.0 mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
A.该合金中铜与镁的物质的量之比是1∶2
B.该浓硝酸中HNO3的物质的量浓度是14.0 mo l·L-1
l·L-1
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是
A.Cu(OH)2 +HCl Cu(OH)2+CH3COOH
B.N aHCO3 +H2SO4 Na2CO3+HCl
aHCO3 +H2SO4 Na2CO3+HCl
C.NaHCO3+NaOH Ca(HCO3)2+NaOH
D.BaCl2+H2SO4 Ba(NO3)2+H2SO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.2K+2H2O=2KOH+H2↑
B.Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3
C.2Cu(NO3)2=2CuO+4NO2↑ +O2↑
D.3CO+Fe2O3=2Fe+3CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com