
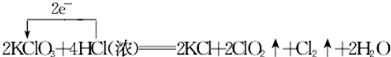 .
.分析 (1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高2价,据此分析;
(2)反应中KClO3为氧化剂,HCl为还原剂;
(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由-1价升高为Cl2中0价,据此计算转移电子物质的量;
(4)根据c=$\frac{1000ρw}{M}$来计算浓盐酸的物质的量浓度;
解答 解:(1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高2价,则电子转移的方向和数目为: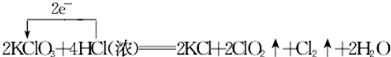
故答案为: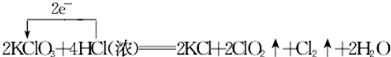 ;
;
(2)KClO3氯元素的化合价降低,是氧化剂,HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高,氯元素被氧化,则氧化剂与还原剂的物质的量之比为1:1,
故答案为:1:1;
(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由-1价升高为Cl2中0价,所以产生22.4L 即1molCl2,转移的电子的物质的量为1mol×2=2mol,
故答案为:2;
(4)由c=$\frac{1000ρw}{M}$可知,c=$\frac{1000×1.19×36.5%}{36.5}$=11.9 mol•L-1,
故答案为:11.9 mol•L-1.
点评 本题考查了氯的化合物的性质、物质的量浓度的计算、氧化还原反应中转移的电子数的计算,明确化合价的变化是分析的关键,难点是消毒效率的计算,题目难度中等,侧重于考查学生阅读题目获取信息的能力、对浓度概念的理解、对氧化还原反应相关知识的运用以及在新情境下综合运用知识解决问题的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 肯定不含I- | B. | 肯定不含NH4+ | C. | 可能含有SO32- | D. | 肯定不含SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
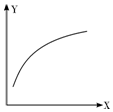 在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )| X | Y | |
| A | 再加入A | B的转化率 |
| B | 再加入C | A的体积分数 |
| C | 减小压强 | A的转化率 |
| D | 升高温度 | 混合气体平均摩尔质量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的转化率变小 | B. | 平衡向正反应方向移动 | ||
| C. | D的物质的量变多 | D. | a>c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池放电时通入空气的电极为负极 | |
| B. | 由于CO32-水解显碱性,电池放电时,电解质溶液的pH逐渐增大 | |
| C. | 电池放电时负极的电极反应式为CH3OH+8OH--6e-═CO32-+6H2O | |
| D. | 电池放电时每消耗1 mol CH3OH转移8 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸的结构简式:C2H4O2 | |
| B. | 乙烯的电子式: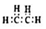 | |
| C. | 硫离子结构示意图: | |
| D. | 氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH-)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝合金的密度小,硬度大,可用作建筑材料 | |
| B. | 食品工业用Na2CO3作焙制糕点的膨松剂 | |
| C. | FeCl3溶液能与Cu反应,可用于腐蚀铜制印刷电路板 | |
| D. | 明矾能生成Al(OH)3胶体,可用作净水剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com