
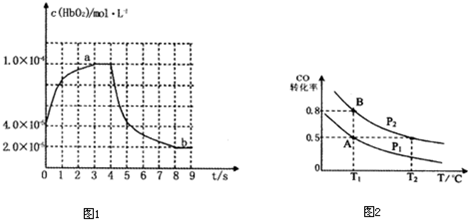
���о����ʱ仯ʱ�����ǿ��ԴӲ�ͬ�ĽǶȡ���ͬ�IJ�������ʶ���ʱ仯ʱ������Ļ�ѧ�����������仯���ݴ��ж����������д������( )
A����ѧ��Ӧ�����ʱ仯��ʵ���Ǿɻ�ѧ�����Ѻ��»�ѧ���γ�
B��ȼ�տɿ��ɡ����桱�������ڲ�������ת��Ϊ���ܡ����ܵ��ͷų���
C����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
D���ڻ�ѧ��Ӧ�У��ƻ��ɻ�ѧ�����յ����������γ��»�ѧ���ͷŵ�����ʱ���÷�Ӧ�����ȷ�Ӧ
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 1 |
| 10000 |
| 1 |
| 10000 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
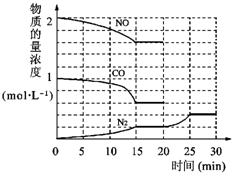 �������ⱸ�������ע���������Լ�����β���ŷŵ�һ����̼��CO�����������NOx������������强��Ϊ������Ⱦ����Ҫ���أ�
�������ⱸ�������ע���������Լ�����β���ŷŵ�һ����̼��CO�����������NOx������������强��Ϊ������Ⱦ����Ҫ���أ� O2+Hb?CO
O2+Hb?CO N2��g��+2CO2��g����H=-113kJ?mol-1
N2��g��+2CO2��g����H=-113kJ?mol-1| 0.4 |
| 15 |
| 0.4 |
| 15 |
 H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯���±���
H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯���±���| �¶�/�� | 400 | 500 | 830 | 1000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | 0.6 |
| A | B | C | D | |
| n��CO2�� | 3 | 1 | 0 | 1 |
| n��H2�� | 2 | 1 | 0 | 1 |
| n��CO�� | 1 | 2 | 3 | 0.5 |
| n��H2O�� | 5 | 2 | 3 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 �籾��������仯�����2009��12��7�տ�Ļ�������ͱ����ԡ���ʷ��������Ҫ�Ļ��顱�����ı�������˵Ļ��顱�ȸ���������ͷ�Σ���Ȼ��������Ծͼ�����������ż��Ľ���������̼���������õ��˹㷺��ͬ���й��������¹��2010��11��5�Ŵ����ĵ�̼֮��--���������ٻص���ǰ���õ�̼�������뵽ÿ���˵�����֮�У���̼��ÿ���˵����Σ�����Դ�����е�ȼ�ϵ���ǵ�̼�о�����Ҫ����
�籾��������仯�����2009��12��7�տ�Ļ�������ͱ����ԡ���ʷ��������Ҫ�Ļ��顱�����ı�������˵Ļ��顱�ȸ���������ͷ�Σ���Ȼ��������Ծͼ�����������ż��Ľ���������̼���������õ��˹㷺��ͬ���й��������¹��2010��11��5�Ŵ����ĵ�̼֮��--���������ٻص���ǰ���õ�̼�������뵽ÿ���˵�����֮�У���̼��ÿ���˵����Σ�����Դ�����е�ȼ�ϵ���ǵ�̼�о�����Ҫ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��14�֣����ǵ����Ϻ����ḻ��Ԫ�أ������仯������о���������������������Ҫ���塣
��1����ͼ��1 molNO2��1 mol CO��Ӧ����CO2��NO�����������仯ʾ��ͼ��д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ ����2�֣�
��2����֪��
N2��g��+O2��g��=2NO��g�� ��H=+180kJ��mol-1
2NO��g��+2 CO��g��=N2��g��+2 CO2��g����H=-746 kJ��mol-1
��ӦCO��g��+1/2O2��g��=CO2��g���ġ�H= kJ��mol-1 ��2�֣�
��3����һ�̶��ݻ�Ϊ2L���ܱ������ڼ���0.2 mol��N2��0.6 mol��H2����һ�������·������·�Ӧ��N2(g)+3H2(g)2NH3(g)��H<0������5����ʱ�ﵽƽ�⣬��ʱ���NH3�����ʵ���Ϊ0.2mol����ǰ5���ӵ�ƽ����Ӧ����v��N2��Ϊ ��ƽ��ʱH2��ת����Ϊ ���÷�Ӧ��ƽ�ⳣ��K= ����6�֣�
��4���ڹ̶�������ܱ������У�1.0��103kPaʱ����ӦN2(g)+3H2(g)2NH3(g) ��H<0��ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
| T/K | 298 | 398 | 498 |
| ƽ�ⳣ��K | 51 | K1 | K2 |
��K1 K2����д��>������=����<������2�֣�
��5�������һ�����ܱ���������˵���ϳɰ���Ӧһ���ﵽƽ��״̬����
������ĸ����2�֣�
a. ������N2��H2��NH3��Ũ��֮��Ϊ1��3��2 b. NH3��Ũ�ȱ��ֲ���
c. ������ѹǿ���ֲ��� d.. ���������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡ÷���и����ܸ�ϰ�ʼ�����ۻ�ѧ�Ծ��������棩 ���ͣ�������
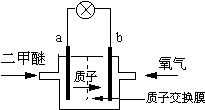
�Ҵ������DZ��㷺ʹ�õ��������ȼ�ϣ���ҵ�����Ҵ���һ�ַ�Ӧԭ��Ϊ��
2CO(g) + 4H2(g)  CH3CH2OH(g) + H2O(g)
��H = ��256.1 kJ��mol��1
CH3CH2OH(g) + H2O(g)
��H = ��256.1 kJ��mol��1
��֪��CO(g) + H2O(g)  CO2(g)+H2(g)
��H= ��41.2 kJ��mol��1
CO2(g)+H2(g)
��H= ��41.2 kJ��mol��1
��1����CO2(g)��H2(g)Ϊԭ��Ҳ�ɺϳ��Ҵ������Ȼ�ѧ����ʽ���£�
2CO2(g) +6H2(g)  CH3CH2OH(g) +3H2O(g)
��H = ��
CH3CH2OH(g) +3H2O(g)
��H = ��
��2������ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⡣
��ij�о�С����ʵ������Ag�C ZSM�C 5Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�������ͼ������ʹ��CO���¶ȳ���800�棬����NO��ת���ʽ��ͣ�����ܵ�ԭ��Ϊ ����n(NO)/n(C O)=1�������£�Ӧ���Ƶ�����¶��� ���ҡ�

���û���̿��ԭ��������������йط�ӦΪ��C (s) +2NO2(g)
 N2 (g) + CO2
(g)��ij�о�С����ij�ܱ������м��������Ļ���̿��NO������( T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
N2 (g) + CO2
(g)��ij�о�С����ij�ܱ������м��������Ļ���̿��NO������( T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
|
�� Ũ��/mol∙L��1 ʱ��/min |
NO |
N2 |
CO2 |
|
0 |
1.00 |
0 |
0 |
|
20 |
0.40 |
0.30 |
0.30 |
|
30 |
0.40 |
0.30 |
0.30 |
|
40 |
0.32 |
0.34 |
0.17 |
|
50 |
0.32 |
0.34 |
0.17 |
I�����ݱ������ݣ���Ӧ��ʼ��20min��v(NO)��ʾ�ķ�Ӧ����Ϊ (������λ��Ч����)��T1��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ (������λ��Ч����)��
II��30min�ı�ijһ��������Ӧ���´ﵽƽ�⣬��ı������������ ����ͼ��ʾCO2���淴Ӧ����[v��(CO2)]�淴Ӧʱ��ı仯��ϵͼ������ͼ�л�����30min�ı���������ʱ����40minʱ���ٴδﵽƽ��ı仯���ߡ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com