
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 任何条件下,等物质的量的Cl2和HCl所含的分子数必相等 | |
| C. | 1LHCl气体一定比1L Cl2气体的质量小 | |
| D. | 22.4LHCl气体的物质的量恰好是11.2LHCl气体的物质的量的二倍 |
分析 A.对于气体物质,同温同压下,体积相同时,物质的量相等;
B.根据N=n×NA分析;
C.没有明确两种气体存在的条件,如果不是相同条件下,两种气体的密度不确定,则质量不能确定;
D.气体状况未知,无法计算气体的物质的量.
解答 解:A.没有明确是否气体物质,如果不是气体物质,则物质的量不一定相等,故A错误;
B.如果Cl2和HCl气体的物质的量相等,则分子数一定相等,故B正确;
C.如果不是相同条件下,两种气体的密度不确定,则质量不能确定,故C错误;
D.氯气与氯化氢气体的状况未知,无法确定其物质的量,故D错误;
故选:B.
点评 本题考查阿伏伽德罗定律及其推论,明确阿伏伽德罗常数使用注意问题是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 在澄清透明的溶液中:H+、Na+、SO42-、Cu2+ | |
| B. | 在Kw/c(OH-)=1 mol•L-1的溶液中:Na+、NH4+、I-、CO32- | |
| C. | 在0.1 mol•L-1NaHSO4溶液中:K+、Fe2+、C1-、NO3- | |
| D. | 在能使甲基橙显黄色的溶液中:Ca2+、Ba2+、Br-、C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.32mol/(L•s) | B. | 0.16mol/(L•s) | C. | 0.8mol/(L•s) | D. | 0.08mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.45mol/(L•s) | B. | v(B)=0.6mol/(L•s) | C. | v(C)=0.5mol/(L•min) | D. | v(D)=0.4mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
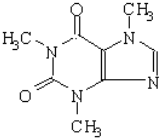
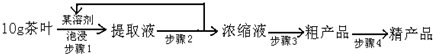
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
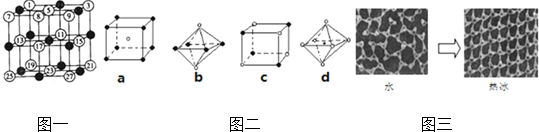
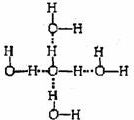
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
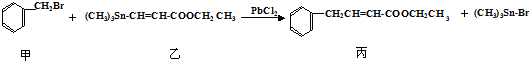
| A. | 分离提纯有机物丙宜在NaOH热溶液中进行 | |
| B. | PbCl2的作用是提高反应物的活性,加快反应速率 | |
| C. | 可用酸性KMnO4溶液检验有机物丙中是否含有机物乙 | |
| D. | 利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在101 kPa时,1 mol H2完全燃烧生成气态水,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度 | |
| C. | 在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.31 kJ•mol-1.若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com