
 向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是
向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是| A. | 在a点对应的溶液中,加入Mg2+、I-、NH4+、NO3-离子仍能大量共存 | |
| B. | 图中B→C的过程中,实际发生的离子方程式为Al(OH)3+OH-=AlO2-+2H2O | |
| C. | 若b、c的纵坐标数值相同,则横坐标数值之比为1:3 | |
| D. | 原溶液中盐酸和AlCl3物质的量的浓度之比为1:3 |
分析 首先发生NaOH+HCl═NaCl+H2O,盐酸反应完毕,再发生反应3NaOH+AlCl3=3NaCl+Al(OH)3↓,最后发生NaOH+Al(OH)3=NaAlO2+2H2O,沉淀溶解,以此来解答.
解答 解:A.B点沉淀最大,溶液中溶质为NaCl,a点的溶液为HCl、AlCl3混合溶液,溶液显酸性,NO3-能氧化I-,不能共存,故A错误;
B.图中B→C的过程是氢氧化铝溶于氢氧化钠溶液,离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故B正确;
C.b、c的纵坐标数值相同,横坐标数值之比不一定为1:3,与纵坐标的值有关,不能是任意点,故C错误;
D.由图可知盐酸完全反应、氯化铝完全反应生成沉淀量最大时消耗氢氧化钠溶液的体积之比为1:3,即消耗氢氧化钠的物质的量之比为1:3,由NaOH+HCl═NaCl+H2O、3NaOH+AlCl3=3NaCl+Al(OH)3↓,可知原溶液中HCl、AlCl3的物质的量之比为1:1,则原溶液中盐酸和AlCl3物质的量的浓度之比为1:1,故D错误;
故选B.
点评 本题以图象形式考查混合物的有关计算,清楚各阶段发生的反应是关键,C选项为易错点,只有唯一的点满足关系.


科目:高中化学 来源: 题型:选择题
| A. | 核内无中子的原子 | |
| B. | 价电子构型为3s23p1 | |
| C. | 最外层电子数等于倒数第三层上的电子数的原子 | |
| D. | N层上无电子,最外层上的电子数等于电子层数的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 装置 | 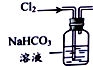 | 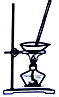 | 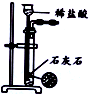 | 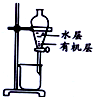 |
| 目的 | 除去Cl2中含有的少量HCl | 蒸发NaCl饱和溶液制备NaCl晶体 | 制取少量纯净的CO2气体 | 分离酒精和水的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 过量的二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| D. | Cl2通入NaOH稀溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在放电时,正极发生的反应是Pb(s)+SO42-(ag)-2e-═PbSO4(s) | |
| B. | 在充电时,电池中硫酸的浓度不断变小 | |
| C. | 在充电时,阴极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(ag) | |
| D. | 在放电时,该电池的负极材料是氧化铅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
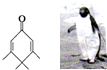 如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )| A. | 若与Penguinone互为同分异构体的酚类且苯环上只有两个取代基的有机物有9种 | |
| B. | Penguinone分子中所有碳原子可能处于同一平面 | |
| C. | Penguinone分子中无酚羟基所以不能使酸性高锰酸钾溶液褪色 | |
| D. | Penguinone分子式为C10H14O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com