
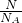 =
=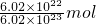 =0.1mol,离子和电子的物质的量之比为0.1mol:0.3mol=1:3,物质的量之比等于微粒个数之比,所以一个离子是由该原子失去三个电子生成的,故电荷数为3;离子数与质子数、中子数之比为=6.02×1022个:6.02×1.3×1023个:6.02×1.4×1023个=1:13:14,所以该离子中含有13个质子、14个中子,故A为27,Z=A-N=27-14=13;
=0.1mol,离子和电子的物质的量之比为0.1mol:0.3mol=1:3,物质的量之比等于微粒个数之比,所以一个离子是由该原子失去三个电子生成的,故电荷数为3;离子数与质子数、中子数之比为=6.02×1022个:6.02×1.3×1023个:6.02×1.4×1023个=1:13:14,所以该离子中含有13个质子、14个中子,故A为27,Z=A-N=27-14=13;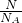 计算离子的物质的量,由电子和离子的物质的量之比求出电荷数;根据离子个数与质子数、中子数之比求出质子数、质量数.
计算离子的物质的量,由电子和离子的物质的量之比求出电荷数;根据离子个数与质子数、中子数之比求出质子数、质量数.

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:《1.1 元素周期表》2010年同步练习(英山一中)(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江西省抚州市黎川一中高一(下)第一次月考化学试卷 (解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com