
2SO2(g)+O2(g) 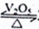 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5不改变该反应的逆反应速率
B.恒压,通入稀有气体,反应速率不变
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是C1mol/L,C2 mol/L,则时间间隔t1(s)~t2(s)内,SO3(g)消耗的平均速率为 V=(C2-C1)/(t2-t1) mol/(L·s)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年广东省高一下期中化学试卷(解析版) 题型:选择题
下列反应中,不能说明SO2是酸性氧化物的是
A.SO2+H2O?H2SO3 B.SO2+2NaOH=Na2SO3+H2O
C.2SO2+O2 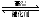 2SO3 D.SO2+CaO=CaSO3
2SO3 D.SO2+CaO=CaSO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能最的变化
B.物质燃烧和中和反应均放出热量
C.分解反应肯定是吸热反应
D.化学反应是吸热还是放热决定于生成物具有的总能最和反应物具有的总能量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
在一定温度下,可逆反应A(g)+3B(g)  2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A. A的生成速率与C分解的速率相等
B.单位时间生成n mol A的同时生成3n mol B
C. A .B.C的浓度不再变化
D. A .B.C的分子个数之比为1:3:2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.离子化合物中,阴、阳离子间存在静电吸引力
B.HF、HCl、HBr和HI的热稳定性和还原性从左到右依次减弱
C.第三周期非金属元素对应的含氧酸从左到右依次增强
D.短周期元素形成离子后,最外层电子数都达到8电子稳定结构
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
工业上用碳还原SiO2制取单质硅会发生如下副反应:SiO2+3C SiC+2CO↑ ,该反应中氧化剂与还原剂的质量比为
SiC+2CO↑ ,该反应中氧化剂与还原剂的质量比为
A.36∶60 B.60∶36 C.1∶2 D.1∶3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:填空题
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ∆H <0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ∆H <0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ∆H <0 (Ⅱ)
2ClNO(g) K2 ∆H <0 (Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向 2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则:平衡后n(Cl2)= mol,NO的转化率а1= ,其它条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是 。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得 1L溶液A,溶液B为0.1mol•L?1的CH3COONa溶液,则两溶液中c(NO3?)、c(NO2-)和c(CH3COO?)由大到小的顺序为 。(已知HNO2的电离常数Ka=7.1×10-4mol•L?1,CH3COOH的电离常数Ka=1.7×10-5mol•L?1)。
可使溶液A和溶液B的pH相等的方法是 。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
B.乙醛和丙烯醛不是同系物,它们与氢气充分反应后的产物也不是同系物
C.氨基酸、蛋白质和氧化铝一样既能与酸反应,又能与碱反应,所以它们都是两性氧化物
D.相同质量的烃,完全燃烧,消耗O2越多,烃中含C量越高
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄冈市高三5月一模理综化学试卷(解析版) 题型:实验题
二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如下:
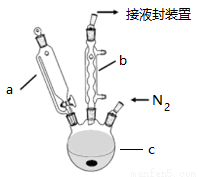
实验原理为:
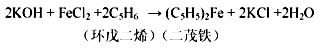
实验步骤为:
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min。
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(密度0.95g/cm3),搅拌。
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜)配成的溶液25ml装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min。
④再从仪器a加入25mL无水乙醚搅拌。
⑤将c中的液体转入仪器d,依次用盐酸、水各洗涤两次,分液得橙黄色溶液。
⑥蒸发橙黄色溶液,得二茂铁粗产品。
⑦……
回答下列问题:
(1)步骤①中通入氮气的目的是: 。
(2)仪器c的名称为: ,其适宜容积应为: 。
a.100ml b.250ml c.500ml
(3)仪器d使用前应进行的操作是: ,请简述该过程: 。
(4)步骤⑦是二茂铁粗产品的提纯,该过程在下图中进行,其操作名称为: 。
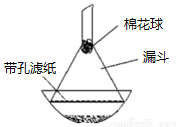
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是 。
(6)最终得到纯净的二茂铁3.7g,则该实验的产率为 (保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com