
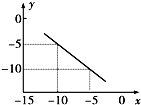
 ��1��25��ʱ����pH=11��NaOH��Һ��pH=4��������Һ��ϣ������û����ҺpH=9����NaOH��Һ��������Һ�������Ϊ
��1��25��ʱ����pH=11��NaOH��Һ��pH=4��������Һ��ϣ������û����ҺpH=9����NaOH��Һ��������Һ�������Ϊ| 10-14 |
| 10-11 |
| 10-14 |
| 10-9 |
| 0.001mol/L��V��-10-4mol/L��V�� |
| V��+V�� |
| 10-12 |
| 10-11 |
| 0.1mol/L��1-0.01mol/L��9 |
| 1+9 |
| 10-12 |
| 10-3 |
| 10-15 |
| 0.01 |


 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.0001mol/L��HCl |
| B��0.00001mol/L��H2SO4 |
| C��0.0000001mol/L��NaOH |
| D����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
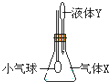 ��ͼʾװ���У���Һ��Y����ƿ�в�ҡ����һ���С�����ʹ�������X��Һ��Y�������ǣ�������
��ͼʾװ���У���Һ��Y����ƿ�в�ҡ����һ���С�����ʹ�������X��Һ��Y�������ǣ������� | A | B | C | D | |
| ����X | NH3 | SO2 | CO2 | HCl |
| Һ��Y | ˮ | ŨNaOH | ϡH2SO4 | ʳ��ˮ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| AԪ��ԭ�ӵĺ���p����������s����������1 |
| BԪ��ԭ��p����������s����������ȣ��Ҳ���AԪ����ͬһ���� |
| Cԭ�����й��ȫ������� |
| DԪ�ص������������������IJ�Ϊ4 |
| E��ǰ�������е縺����С��Ԫ�� |
| F�����ڱ��ĵ����� |
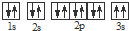 ������
��Υ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| |�¶�/�� | 700 | 900 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��CO�ϳɼ״���CH3OH���Ļ�ѧ��Ӧ����ʽΪCO��g��+2H2��g��?CH3OH��g����H��0��������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
��CO�ϳɼ״���CH3OH���Ļ�ѧ��Ӧ����ʽΪCO��g��+2H2��g��?CH3OH��g����H��0��������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A������Ӧ���ʣ�v��a����v��c����v��b����v��d�� | ||||||||
| B��ƽ��ʱa��һ����n��CO����n��H2��=1��2 | ||||||||
| C��ƽ�ⳣ����K��a����K��c����K��b��=K��d�� | ||||||||
D��ƽ��Ħ��������
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com