
【题目】下表是氧族部分元素的相关性质。
元素 性质 | 8O | 16S | 34Se | 52Te |
主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
原子半径 | 逐渐增大 | |||
单质与H2 反应情况 | 点燃时 易化合 | 加热 化合 | 加热 难化合 | 不能 直接化合 |
请回答下列问题:
(1)硒在周期表中位置____。
(2)碲的化合价可能有____。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是__________(填化学式)。
(4)氢硒酸有较强的____(填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_____________。
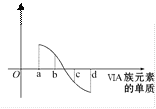
(5)氧族元素单质与H2反应过程中的焓变如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表___,d代表___(均写单质名称)。
【答案】 第四周期第ⅥA族 -2、+4、+6 H2Te、H2Se、H2S 还原性 2H2Se+O2===2Se↓+2H2O 硒 氧气
【解析】本题主要考查元素周期律。
(1)硒在周期表中位置:第四周期第ⅥA族。
(2)碲的化合价与硫相似,可能有-2、+4、+6。
(3)同主族元素硫、硒、碲的氢化物水溶液的酸性与元素的非金属性呈负相关,非金属性Te<Se<S,所以氢化物水溶液的酸性由强至弱的顺序是H2Te、H2Se、H2S。
(4)硒元素的非金属性比硫弱,氢化物的还原性比硫化氢强,氢硒酸有较强的还原性,因此放在空气中易变质,其可能发生的反应与硫化氢相似,反应的化学方程式为2H2Se+O2===2Se↓+2H2O。
(5)元素的非金属性越强,元素单质与H2反应过程中的焓变越小,则b代表硒,d代表氧气。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】碳及其化合物与人类的生活、生产紧密联系。
(1)已知2g甲烷完全燃烧生成稳定的氧化物时放出Q kJ的热量,写出表示甲烷燃烧热的热化学方程式:___________
(2)已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+130 kJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1。断开1 mol H—H键、O===O键分别需要吸收436 kJ、496 kJ的热量,则断开1 mol O—H键需要吸收的热量为___________
A.332 kJ B.462 kJ C.118 kJ D.360 kJ
(3)以CO2和H2O为原料制备HCOOH和O2的原电池原理如图.

电极a为_____(填“正”或“负”)极,电极b发生的电极反应式是:___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以将反应Zn+Br2= ZnBr2设计成蓄电池,下列4个电极反应:
①Br2+ 2e-= 2Br- ②2Br-- 2e-= Br2③Zn – 2e-= Zn2+④Zn2++ 2e-= Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是
A.④和①B.②和①C.③和①D.②和③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋葛洪在《抱朴子》中写道“扶南生金刚,生水底石上,如钟乳状,体似紫石英,可以刻玉,人没水取之,虽铁椎之亦不能伤.”文中所述“金刚”可能为
A.结晶氯化钠B.金刚石C.碳酸钠D.二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 使用pH试纸测量气体的酸碱性时可以润湿
B. 实验室用氢氧化钠溶液除去氯气中的少量HCl
C. 蒸馏操作时,温度计水银球应插入混合液中
D. 配制溶液定容时,俯视容量瓶的刻度线,则所配制溶液的浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从下图中选择:
(1)金属钠的晶胞模型是____________,每个Na原子周围有________个紧邻的Na原子。
(2)金属铜的晶胞模型是____________,每个Cu原子周围有________个紧邻的Cu原子。

(3)金属导电靠_________________________________, 电解质溶液导电靠____________________________ ;
(4)根据下列叙述,判断一定为金属晶体的是___________________。
A.由分子间作用力形成,熔点很低
B.由共价键结合形成网状晶体,熔点很高
C.固体有良好的导电性、导热性和延展性
(5)已知下列金属晶体: Po、K、Mg、Au,其堆积方式为:
①简单立方堆积的是________;
②体心立方堆积的是________;
③六方堆积的是 ________;
④面心立方堆积的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明硫酸为强酸的实验事实是
A. 能与酸碱指示剂作用 B. 0.1mol/L的硫酸中,测得c(H+)=0.2mol/L
C. 能与金属锌反应生成氢气 D. 能与食盐固体共热产生气体氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
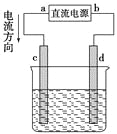
A. a为负极,b为正极
B. a为阳极,b为阴极
C. 电解过程中,d电极质量增加
D. 电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C的结构简式如图所示。

(1)维生素C的分子式是_______________。
(2)维生素C___________溶于水(填“易”或“难”)。
(3)在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有______性。
(4)在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到溶液蓝色退去,说明维生素C具有___________性。
(5)中学生每天需补充约60 mg维生素C,下列物质中含有丰富维生素C的是____________。
A.辣椒 B.鸡蛋 C.米饭 D.青霉素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com