
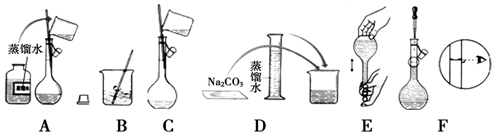
| A. | 洗净的容量瓶可以放进烘箱中烘干 | |
| B. | 用磨口玻璃瓶保存NaOH溶液 | |
| C. | 用苯萃取溴水中的溴时,溴的苯溶液从分液漏斗的下口放出 | |
| D. | 用二硫化碳清洗残留在试管壁上少量的硫粉 |
分析 A.容量瓶不需要干燥;
B.氢氧化钠溶液与二氧化硅反应,不能使用玻璃塞;
C.苯的密度小于水,在混合液上层;
D.硫粉易溶于二硫化碳.
解答 解:A.容量瓶中有少量水不影响配制结果,所以容量瓶不影响烘干,故A错误;
B.玻璃塞中的二氧化硅与NaOH溶液反应,不能用玻璃塞的试剂瓶盛放碱液,应该用橡胶塞,故B错误;
C.苯的密度比水小,用苯除去溴水中的溴时,有机层在上层,溴的苯溶液应该从分液漏斗的上口倒出,故C错误;
D.由于二硫化碳能够溶解硫单质,可用二硫化碳清洗残留在试管壁上少量的硫粉,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及仪器构造及使用、分液、试剂保存等知识,明确常见化学实验基本操作方法为解答关键,试题侧重基础知识的考查,培养了学生的化学实验能力.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2+3H2=2NH3属于自然固氮 | |
| B. | 固氮属于氧化还原反应 | |
| C. | 俗语“雷雨发庄稼”毫无科学道理 | |
| D. | 氨气溶于水得到的溶液能导电,所以NH3是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| B. | 由NaCl制漂白剂:NaCl(aq)$\stackrel{电解}{→}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| C. | 由铝土矿冶炼铝:铝土矿$→_{Na_{3}AlF_{6}}^{电解}$Al | |
| D. | 合成NH3:NH4Cl和Ca(OH)2固体$\stackrel{△}{→}$NH3$\stackrel{碱石灰}{→}$纯净干燥的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
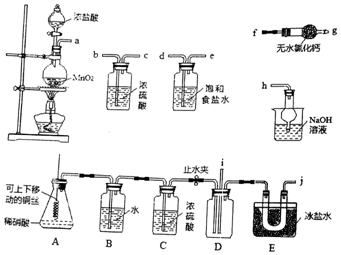
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 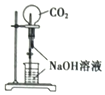 喷泉实验 | B. |  配制一定物质的量浓度的NaCl溶液 | ||
| C. | 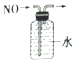 排水法收集NO | D. |  碳酸氢钠受热分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
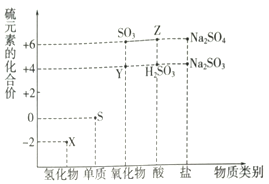 利用元素的化合价推测物质的性质是化学研究的重要手段.
利用元素的化合价推测物质的性质是化学研究的重要手段.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 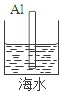 | B. | 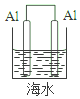 | C. | 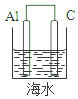 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com