
| A. | 铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 明矾能水解生成Al(OH)3胶体,可用作水的消毒剂 | |
| C. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 | |
| D. | 氯化铝是一种电解质,可用于电解法制铝 |
分析 A.在海轮外壳上装若干铜块,构成原电池,Fe为负极;
B.明矾不具有强氧化性;
C.Cu与氯化铁反应生成氯化亚铁、氯化铜;
D.氯化铝为共价化合物,不能电解氯化铝制备Al.
解答 解:A.在海轮外壳上装若干铜块,构成原电池,Fe为负极,则加快海轮外壳腐蚀,故A错误;
B.明矾不具有强氧化性,可净化水,但不能消毒,故B错误;
C.Cu与氯化铁反应生成氯化亚铁、氯化铜,则FeCl3溶液能与Cu反应,可用于蚀刻印刷电路,故C正确;
D.氯化铝为共价化合物,溶于水可导电,属于电解质,不能电解氯化铝制备Al,可电解熔融氧化铝冶炼Al,故D错误;
故选C.
点评 本题考查常见金属及化合物的性质,为高频考点,把握物质的性质、发生的反应、原电池、性质与用途等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | N2、O2和Cl2分子中既含有σ键,又含有π键 | |
| B. | PCl3分子中,中心原子采取SP3杂化方式 | |
| C. | CS2、H2O、C2H2都是直线型分子 | |
| D. | CH4、CCl4、C6H6都是只含有极性键的非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3═Na++H++CO32- | B. | NaHSO4═Na++H++SO42- | ||
| C. | Al2(SO4)3═Al3++SO42- | D. | NH3•H2O═NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖原与纤维素互为同分异构体,与淀粉互为同系物 | |
| B. | 糖原能溶于水,有甜味 | |
| C. | 糖原水解的最终产物是葡萄糖 | |
| D. | 糖原具有还原性,是还原性糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
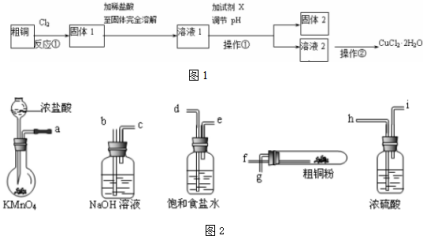
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 世博会前期,净化自来水时加入ClO2作为消毒剂 | |
| B. | 世博会期间,利用可降解的“玉米塑料”替代一次性饭盒,可防止产生白色污染 | |
| C. | 世博停车场安装催化光解设施,可将汽车尾气中的CO和NO反应生成无毒气体 | |
| D. | 世博会中国馆一“东方之冠”使用的钢筋混凝土属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 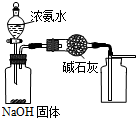 用图装置制取干燥纯净的NH3 | |
| B. |  用图装置实验室制备Fe(OH)2 | |
| C. |  用图装置可以完成“喷泉”实验 | |
| D. |  用图装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com