
| ||
| ||
| ||
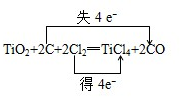 ,故答案为:
,故答案为: ;Cl2;C;
;Cl2;C;

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:

| 实验内容 | 试剂 | 实验现象 |
| 验证氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
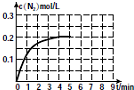 研究化学反应,不仅要关注反应的速率、方向性,还要关注反应进行的限度以及反应过程中的能量变化.
研究化学反应,不仅要关注反应的速率、方向性,还要关注反应进行的限度以及反应过程中的能量变化.| 0 | 1min | 2min | 4min | 5min | |
| 130℃ | 0.50mol | 0.35mol | 0.25mol | 0.10mol | 0.10mol |
| 180℃ | 0.50mol | 0.30mol | 0.18mol | 0.15mol |
| c2(N2)?c2(H2O) |
| c2(NH3)?c(NO)?c(NO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ⑨ | ① | ② | ⑧ | ||||
| 3 | ③ | ⑦ | ④ | ⑤ | ⑥ | |||
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、邻羟基苯甲醇分子中所有的原子可能在同一平面 |
| B、用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① |
| C、邻羟基苯甲酸的化学式为C7H6O3 |
| D、1mol邻羟基苯甲醛最多能与3mol H2发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com