
【题目】(12分)有X、Y、Z三种短周期元素,已知X的气态氢化物的分子式为H2X,该氢化物的相对分子质量与X最高价氧化物的相对分子质量之比为17∶40,X原子核内质子数与中子数相等;Y与X可形成离子化合物Y2X,Y的阳离子的电子层结构与Ne相同。Z与X处于同一周期,其气态单质是双原子分子,两原子共用一对电子。
(1)写出各元素的符号:X______,Y______,Z______。
(2)X的相对原子质量为____________,其离子的结构示意图为________。
(3)Y单质在空气中燃烧的化学方程式是________________________,该生成物与水反应的化学方程式是______________________。
(4)X与氢气化合的产物的电子式为________。
【答案】 S Na Cl 32 ![]() 2Na+O2
2Na+O2![]() Na2O2 2Na2O2+2H2O===4NaOH+O2↑ H
Na2O2 2Na2O2+2H2O===4NaOH+O2↑ H ![]()
【解析】试题分析:X的气态氢化物的分子式为H2X,则X的最低价是-2,最高价是+6,X最高价氧化物的化学式为XO3,该氢化物的相对分子质量与X最高价氧化物的相对分子质量之比为17∶40,即![]() ,x=32,X原子核内质子数与中子数相等,x是S元素。Y与X可形成离子化合物Y2X,Y是+1价元素,Y的阳离子的电子层结构与Ne相同,故Y是Na元素;Z与X处于同一周期,其气态单质是双原子分子,两原子共用一对电子,Z是Cl元素。
,x=32,X原子核内质子数与中子数相等,x是S元素。Y与X可形成离子化合物Y2X,Y是+1价元素,Y的阳离子的电子层结构与Ne相同,故Y是Na元素;Z与X处于同一周期,其气态单质是双原子分子,两原子共用一对电子,Z是Cl元素。
解析:根据以上分析,(1)各元素的符号:X是 S,Y是Na,Z是Cl。
(2)S的相对原子质量为32, ![]() 的结构示意图为
的结构示意图为![]() 。
。
(3)钠在空气中燃烧生成过氧化钠的化学方程式是2Na+O2 ![]() Na2O2,过氧化钠与水反应生成氢氧化钠和氧气,化学方程式是2Na2O2+2H2O===4NaOH+O2↑。
Na2O2,过氧化钠与水反应生成氢氧化钠和氧气,化学方程式是2Na2O2+2H2O===4NaOH+O2↑。
(4)S与氢气生成硫化氢,硫化氢的电子式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是

A.该装置能量转化形式是电能转化为化学能
B.负极反应式为:CH2=CH2-2e-+H2O=CH3CHO +2H+
C.每有0.1 mol O2反应,则向负极迁移的H+的物质的量为0.4 mol
D.电子移动方向:电极a→磷酸溶液→电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸乙酯可用作食用香料。某小组用如下装置制备苯甲酸乙酯
反应原理: (苯甲酸乙酯)+H2O
(苯甲酸乙酯)+H2O
产物和部分反应物相关数据如下:
物质 | 苯甲酸 | 乙醇 | 苯甲酸乙酯 |
熔点/℃ | 122.1 | -117.3 | -34.6 |
沸点/℃ | 249 | 78.3 | 213 |

实验步骤:
①在B中加入的物质有:12.2g苯甲酸、10mL乙醇、10mL浓硫酸和沸石;
②按图甲安装好仪器,水浴加热,回流2小时;
③冷却后将B中液体与30mL水混合,并分批加入碳酸钠粉末;
④分液,取出有机层并加入适量MgSO4摇匀;
⑤按图乙装置安好仪器,加热精馏④所得有机物,收集产品。
回答下列问题:
(1)仪器C的名称______________。
(2)步骤① 若加热后才发现未加沸石,应采取的措施是________;步骤② 采取水浴加热的优点是______。
(3)步骤③ 为了预防液体因瞬时放出大量热而飞溅,将有机物与水混合的操作是____________。
(4)步骤④分液时除了要用到烧杯,还需要的主要玻璃仪器有__________,使用该仪器之前需要进行的操作是__________;无水MgSO4的作用是___________。
(5)步骤⑤收集馏分应控制的最佳温度为____________。
(6)为了提高苯甲酸乙酯的产率,可以采取的措施_________(任填一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,烧杯中的溶质均足量,a、b、c、d、e均为石墨电极,通电一段时间后,a电极上有红色物质析出,以下说法正确的是

A.B烧杯中加一定量的KCl固体可使溶液恢复原状[
B.b电极周围溶液变红
C.A烧杯内Cu2+浓度降低
D.d电极上可以析出使湿润的淀粉KI试纸变蓝的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。

(1)汞位于第六周期,且与锌同族,写出Hg的最外层电子排布式________。
(2)Ge元素属于_____(从下列选项中选择)
A.s区 B.类金属 C.非金属 D.过渡金属 E.准金属
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是________
(4)NH3也常作制冷剂,其分子构型是______,NH3的沸点(239.6℃)高于N2沸点的主要原因是_____
(5)图示材料的理想化学式(无空位时)为_____,若Y(钇)元素的化合价为+3,则Cu的平均化合价为___
(6)金属铜为立方晶胞,空间利用率为74%,晶胞边长为a cm,铜的相对原子质量为63.5,阿伏伽德罗常数为NA。则金属铜的晶体密度ρ=_____g/cm3(只含一个系数,用a、NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是

A.MOH是一种弱碱
B.在x点,c(M+)=c(R+)
C.稀释前,c(ROH)=10 c(MOH)
D.稀释前MOH溶液和ROH溶液中由水电离出的c(OH﹣)后者是前者的 10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1mol·L﹣1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A.该混合溶液pH=7.0
B.原HA溶液中:c(HA)>c(H+)>c(A﹣)
C.图中X表示HA,Y表示OH﹣,Z表示H+
D.混合溶液中:c(X)+x(A﹣)=c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是熔点最高的金属,是重要的战略物资。自然界中钨主要存在于黑钨矿中,其主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、As的化合物。由黑钨矿冶炼钨的工艺流程如下:
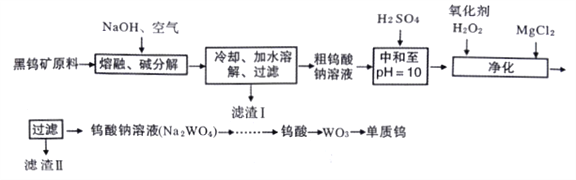
已知:
①滤渣I的主要成份是Fe2O3、MnO2。
②上述流程中,钨的化合价只有在最后一步发生改变。
③常温下钨酸难溶于水。
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为____,请写出MnWO4在熔融条件下发生碱分解反应生成Fe2O3的化学方程式__________。
(2)上述流程中向粗钨酸钠溶液中加硫酸中和至pH=10后,溶液中的杂质阴离子确SiO32-、HAsO32-、HAsO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为____,滤渣Ⅱ的主要成分是____。
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。下图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线,则:
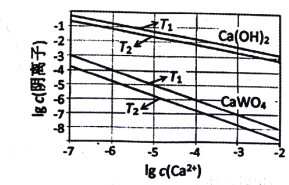
①T1 _____T2(填“>”或“<”)T1时Ksp(CaWO4)=____。
②将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚对苯二甲酸乙二酯(J)具有良好的力学性能,其薄膜的伸拉强度是聚乙烯薄膜的9倍。它的合成路线如下:
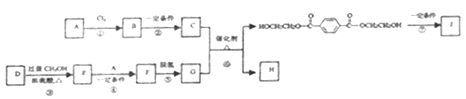
已知:
①![]()
②酯与醇可发生如下酯交换反应:RCOOR′+R〞OH ![]() RCOOR〞+R′OH(R、R′、R〞代表烃基)
RCOOR〞+R′OH(R、R′、R〞代表烃基)
(1)A的产量标志着一个国家石油化工发展水平,反应①的反应类型为______________。
(2)C的分子式是C2H6O2,是汽车防冻液的主要成分。反应②的试剂和反应条件是____________。
(3)D的分子式是C6H6O4,是一种直链结构的分子,核磁共振氢谱有3种峰,D种含有的官能团是______。
(4)F的结构简式是__________________。
(5)反应⑥的化学方程式是_________________。
(6)反应⑦为缩聚反应,反应⑦的化学方程式是_________________。
(7)G是一种同分异构体,G′为甲酸酯,核磁共振氢谱有3种峰且1mol该有机物酸性条件下水解产物能与2molNaOH反应。G′的结构简式为______________。
(8)以对二甲苯、甲醇为起始原料,选用必要的无机试剂合成G,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com