
分解水制氢气的工业制法之一是硫——碘循环,主要涉及下列反应:
I SO2+2H2O+I2→H2SO4+2HI
II 2HI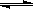 H2+I2
H2+I2
III 2H2SO4 → 2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是_________
a.反应III易在常温下进行 b.反应I中SO2还原性比HI强
c.循环过程中需补充H2O d.循环过程中产生1molO2的同时产生1molH2
(2)一定温度下,向2L密闭容器中加入1molHI(g),发生反应II,H2物质的量随时间的变化如图所示。

0—2min内的平均反应速率v(HI)=
_________ 。该温度下,反应2HI(g)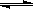 H2(g)+I2(g)的平衡常数表达式为K=_______________________。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_________是原来的2倍。
H2(g)+I2(g)的平衡常数表达式为K=_______________________。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_________是原来的2倍。
a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)SO2在一定条件下可氧化生成SO3,其主反应为:2SO2 (g) + O2(g)  2SO3(g)
+ Q,若此反应起始的物质的量相同,则下列关系图正确的是_________ (填序号)
2SO3(g)
+ Q,若此反应起始的物质的量相同,则下列关系图正确的是_________ (填序号)

实际工业生产使用的条件是:常压、____________________________________选择该条件的原因是__________________。
(4)实际生产用氨水吸收SO2生成亚硫酸的铵盐。现取a克该铵盐,若将其中的SO2全部反应出来,应加入18.4 mol/L的硫酸溶液的体积范围为______________。
(1)bc(2分)
(2)0.05mol·L-1·min-1;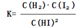 ;b (各1分)
;b (各1分)
(3)bd;五氧化二钒、500℃;加快反应速度。(共5分)
(4)a/116×18.4~a/198×18.4 (2分)
【解析】
试题分析:(1)a.反应III2H2SO4 → 2SO2+O2+2H2O是分解反应,要在高温下进行。b.根据还原剂的还原性强于还原产物的还原性,故反应I中SO2还原性比HI强,正确。c.水在循环过程中始终消耗,故需补充H2O,正确。d.根据电子守恒,循环过程中产生1molO2转移4mol电子,同时产生2molH2,错误。故选bc。
(2)根据平均反应速率v(HI)=2v(H2)=2*0.1/(2*2 )= 0.05mol·L-1·min-。该温度下,反应2HI(g)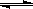 H2(g)+I2(g)的平衡常数表达式为K=
H2(g)+I2(g)的平衡常数表达式为K=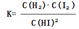 。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,根据反应前后体积不变这个特点可知与原平衡是等效平衡,则HI的平衡浓度是原来的2倍,而平衡常数只与温度有关,温度不变,平衡常数也不变,平衡时H2的体积分数相同。
。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,根据反应前后体积不变这个特点可知与原平衡是等效平衡,则HI的平衡浓度是原来的2倍,而平衡常数只与温度有关,温度不变,平衡常数也不变,平衡时H2的体积分数相同。
(3)根据反应2SO2 (g) + O2(g)  2SO3(g)
+ Q的特点,正反应体积减小,放热反应,故关系图正确的是bd。实际工业生产还要根据设备的成本,反应速率及催化剂的适宜温度综合考虑故使用的条件是:常压、五氧化二钒、500℃;选择该条件的原因是加快反应速度。
2SO3(g)
+ Q的特点,正反应体积减小,放热反应,故关系图正确的是bd。实际工业生产还要根据设备的成本,反应速率及催化剂的适宜温度综合考虑故使用的条件是:常压、五氧化二钒、500℃;选择该条件的原因是加快反应速度。
(4)亚硫酸的铵盐正盐和酸式盐两种情况。若a克分别是两种铵盐时,应加入18.4 mol/L的硫酸溶液的体积设为v,则
(NH4)2SO3 -----H2SO4 2NH4HSO3----H2SO4
a/116 a/116 a/99 a/198
v=a/116×18.4 v=a/198×18.4,应加入18.4 mol/L的硫酸溶液的体积范围为a/198×18.4----a/116×18.4。
考点:本题考查化学平衡状态,化学平衡常数,反应速率计算,用极值法解决化学计算。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
| ||
| 熔融 |
| ||
| 熔融 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:
|
| 开始沉淀 | 完全沉淀 |
| Fe3+ | 2.7 | 3.7 |
| Mn2+ | 8.3 | 10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:
![]()
![]()
(3)由上可知,表示H2燃烧热的热化学方程式是__________________________。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
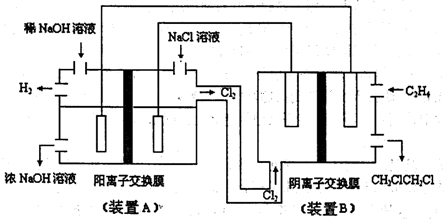
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年银川二中高三模拟(二)试题理综化学 题型:填空题
【化学选修2:化学与技术】(15分)
工业上为了使原料和能量得到充分的利用,常常采用循环操作。
I、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。MnFe2O4的制备:

已知Fe3+、Mn2+沉淀的pH如右表所示。
|
|
开始沉淀 |
完全沉淀 |
|
Fe3+ |
2.7 |
4.2 |
|
Mn2+ |
8.3 |
10.4 |
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比应为 。
(2)控制pH的操作中m的值为 。
II、用MnFe2O4热化学循环制取氢气:


(3)由上可知,H2燃烧的热化学方程式是 。
(4)该热化学循环制取氢气的优点是 (填字母编号)。
A.过程简单、无污染 B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
III、工业上可用H2、HCl通过下图的循环流程制取太阳能材料高纯硅。

反应①
反应②:
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是 。
查看答案和解析>>
科目:高中化学 来源:重庆市2010届高三下学期5月月考(理综化学部分) 题型:填空题
(15分)工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
MnFe2O4的制备:

|
|
开始沉淀 |
完全沉淀 |
|
Fe3+ |
2.7 |
3.7 |
|
Mn2+ |
8.3 |
10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:


(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
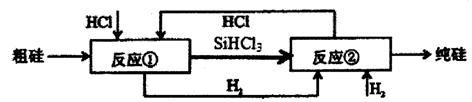
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com