
下列关于容量瓶及其使用方法的叙述,正确的是
A.是配制一定物质的量浓度的溶液的专用仪器
B.容量瓶可以用来加热
C.能用容量瓶贮存配制好的溶液
D.可以用500mL容量瓶配制250mL溶液
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:2014-2015湖南省高二上学期期中考试化学(文)试卷(解析版) 题型:选择题
下列关于食品添加剂的叙述中不正确的是
A.醋可同时用作防腐剂和调味剂 B.亚硝酸钠可能致癌
C.我国应该禁止使用味精 D.苯甲酸钠可用作食品防腐剂
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中考试化学(理)试卷(解析版) 题型:选择题
下列电离方程式错误的是
A.Al2(SO4)3=2Al3+ + 3SO42-
B.NaHCO3=Na+ + H+ + CO32-
C.Ba(OH)2= Ba2+ + 2 OH-
D.NaHSO4=Na++H++SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省郴州市高一上学期期中考试化学试卷(解析版) 题型:选择题
0.1 mol NaHCO3中含有
A.0.2 mol Na+ B.0.2 mol CO32-
C.6.02×1023个 O原子 D.0.1 mol H原子
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省郴州市高一上学期期中考试化学试卷(解析版) 题型:选择题
将饱和氯化铁溶液滴入沸水中,形成的分散系属于
A.溶液 B.悬浊液 C.乳浊液 D.胶体
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市四校高二12月联考化学试卷(解析版) 题型:填空题
(12分)盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。已知室温下:Ka(CH3COOH)=1.7×10-5 mol·L-1 ;H2CO3的电离常数Ka1=4.2×10-7mol·L-1 、 Ka2=5.6×10-11mol·L-1
(1)①请用离子方程式解释碳酸氢钠水溶液显碱性的原因 。
②常温下,物质的量浓度相同的下列四种溶液:
a、碳酸钠溶液 b、醋酸钠溶液 c、氢氧化钠溶液 d、氢氧化钡溶液
其PH由大到小的顺序是: (填序号)。
(2)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应的溶液中水的电离程度由大到小的顺序是 ;该醋酸溶液稀释过程中,下列各量一定变小的是 。

a.c(OH-) b.c(H+)
c. d.
d.
(3)以0.10 mol·L-1NaOH为标准液,测定某盐酸的浓度。取20.00 mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | 氢氧化钠溶液的浓度 (mol·L-1) | 滴定完成时,氢氧化钠溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 24.12 | 20.00 |
2 | 0.10 | 23. 88 | 20.00 |
3 | 0.10 | 24.00 | 20.00 |
①滴定达到终点的标志是___________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为__________________。
(4)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13,则:
①该温度下水的离子积常数Kw= mol2·L-2。
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市四校高二12月联考化学试卷(解析版) 题型:选择题
已知在25℃时,Ksp(AgCl)=1.8×10—10,Ksp(AgI)=8.3×10—17,下列说法错误的是
A.在100mL0.01mol/LKCl溶液中,加入1mL0.01mol/LAgNO3溶液,有沉淀析出
B.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度减小
C.由于Ksp(AgCl)>Ksp(AgI),AgCl 沉淀在一定条件下可转化为AgI沉淀
D.往氯化银的悬浊液中加硝酸银固体,c(Cl—)、c(Ag+)均减小
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省许昌市四校高一上学期第三次联考化学试卷(解析版) 题型:填空题
(8分)分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
物质 | 需加入的试剂 | 有关离子方程式 |
FeSO4 (Fe2(SO4) 3) | ||
Mg(Al) | ||
CO2 (HCl) | ||
SiO2(CaCO3) |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:填空题
(15分)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生如下反应:
CO2 (g)+CH4(g) 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K=__________
②已知: 《1》CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= 890.3 kJ·mol-1
890.3 kJ·mol-1
《2》CO(g)+H2O (g)=CO2(g)+H2 (g) △H=+2.8 kJ·mol-1
《3》2CO(g)+O2(g)=2CO2(g) △H= 566.0 kJ·mol-1
566.0 kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H=________________
2CO(g)+2H2(g) 的△H=________________
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是 。
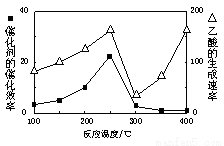
②为了提高该反应中CH4的转化率,可以采取的措施是 。
③将Cu2Al2O4溶解在稀硝酸中的离子方程式为 。
(3)①Li2O、Na2O、MgO均能吸收CO2。①如果寻找吸收CO2的其他物质,下列建议合理的是_____。
A.可在碱性氧化物中寻找
B.可在ⅠA、ⅡA族元素形成的氧化物中寻找
C.可在具有强氧化性的物质中寻找
②Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是 。
(4)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:CO2+H2O CO+H2+O2
CO+H2+O2
高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

CO2在电极a放电的反应式是__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com