
����Ŀ����ҵ���Ժ����ƼΪ�����������������ƣ�Na2S2O5�������Ʊ�����������ͼ��

��֪����ӦII����2NaHSO3=Na2S2O5+H2O�ȶಽ��Ӧ��
��1����ӦI�Ļ�ѧ����ʽΪ___________________________________________��
��2����������ʱ������Ӧ�Ļ�ѧ����ʽΪ_______________________________________________��
��3����֪Na2S2O5��ϡ���ᷴӦ�ų�SO2�������ӷ���ʽΪ________________��
��4����ӦIʱӦ��ͨ������Ϊ__________������ƷX�Ļ�ѧʽ��_________________��
��5��Ϊ�˼��ٲ�ƷNa2S2O5�����ʺ���������Ʒ�ӦII���������������ʵ���֮��ԼΪ______��
���𰸡� NaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl 2CuS+3O2����2CuO+2SO2 S2O52-+2H+=2SO2��+H2O NH3 CuSO45H2O 2�U1
��������������Ҫ���������ҵ���Ժ����ƼΪ�����������������ƣ�Na2S2O5���Ĺ������̵����ۡ�
��1����ӦI�Ļ�ѧ����ʽΪNaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl��������ΪNH3+CO2+H2O=NH4HCO3��NaCl+ NH4HCO3=NaHCO3��+NH4Cl��
��2����������ʱ���ɵĺ�ɫ����������ͭ��ͬʱSת��ΪSO2��������Ӧ�Ļ�ѧ����ʽΪ2CuS+3O2![]() 2CuO+2SO2��
2CuO+2SO2��
��3����֪Na2S2O5��ϡ���ᷴӦ�ų�SO2�������ӷ���ʽΪS2O52-+2H+=2SO2��+H2O��
��4��NH3���ܽ�ȴ���CO2�����Է�ӦIʱӦ��ͨ������ΪNH3���������ɫ��������ͭ��Ӧ��������ͭ������ƷX�Ļ�ѧʽ��CuSO45H2O��
��5��Ϊ�˼��ٲ�ƷNa2S2O5�����ʺ������ӻ�ѧʽNa2S2O5���Կ�������Ʒ�ӦII���������������ʵ���֮��ԼΪ2:1��


 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaCl��CaCl2��AlCl3������Һ���ֱ���������AgNO3��Һ��Ӧ�������������ʵ����ʵ�����ȣ������ɳ��������ʵ���֮�������������ɳ�����������ȣ���������Һ���������ʵ����ʵ���֮���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ�������ӷ�Ӧ����
A. ����������ȼ�� B. ������̼ͨ������ʯ��ˮ��
C. �Ȼ�����Һ�еμ���������Һ D. п������ϡ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��һ��������N2��H2��Ӧ����NH3����ش�
������Ӧ���������ΪE1���������������ΪE2����E1��E2����÷�ӦΪ________(����ȡ����ȡ�)��Ӧ��
����֪��1 mol H��H����1 mol N��H����1 mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ________________��
(2) N2H4��H2O2��Ͽ�������ƽ�������֪��16 gҺ̬N2H4������������Ӧ����N2(g)��H2O(l)���ų�310.6 kJ��������2H2O2(l)===O2(g)��2H2O(l)����H����196.4 kJ��mol��1����ӦN2H4(g)��O2(g)===N2(g)��2H2O(l)�Ħ�H��____________kJ��mol��1��N2H4��H2O2��Ӧ����N2(g)��H2O(l)���Ȼ�ѧ����ʽΪ_______________________________________��
(3)ʵ������50 mL 0.50 mol��L��1������50 mLijŨ�ȵ�NaOH��Һ����ͼ��ʾװ���з�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���װ�����������ԵĴ�������һ����ȱ��һ�ֲ���������������������Ϊ____________��ʵ�����ṩ��0.50 mol��L��1��0.55 mol��L��1����Ũ�ȵ�NaOH��Һ��Ӧѡ��_____________mol��L��1��NaOH��Һ����ʵ�顣

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������Թ� �������� ���ձ� ����ƿ ������ ������ƿ ����Ͳ ���þƾ���ֱ�Ӽ��ȵ���
A. �٢ڢۢܢ� B. �٢ڢۢܢ� C. �٢ڢ� D. �ڢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���X�ķ���ʽΪC3H6O2������������������ˮ�⣬ˮ�����ֻ�����֣��������ֲ������Է���������ȣ����л���X�Ľṹ��ʽ�ǣ� ��
A.CH3CH2COOHB.CH3COOCH3
C.HCOOCH2CH3D.HOCH2CH2CHO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��ר���о�������Ԫ�ؼ���ijЩ������IJ������ʡ�����������Ϣ���£�
�����ԣ�H2SO4>H2SeO4>H2TeO4
��������������������Խ��Խ�ѣ�������������ֱ�ӻ���
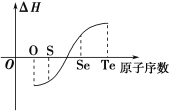
����Ԫ�صĵ������ɵ����ʵ������⻯����ʱ��������ͼ��ʾ��
������������⣺
��1��H2���ϵķ�Ӧ______����(��ų��������ա�)��
��2����֪H2Te�ֽⷴӦ�Ħ�S>0�������ΪʲôTe��H2����ֱ�ӻ���_________________________________________��
��3������������Ϣ���ܹ�˵����Ԫ�طǽ�����ǿ����Ԫ�ص���________(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ��������װ�õ���ţ� 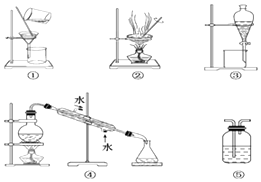
��1������Na2CO3��Һ��CH3COOC2H5��������ˮ��Һ�壩��ѡ �� ��������Ϊ ��
��2����CCl4��ȡ��ˮ�еĵ⣬ѡ �� ��������Ϊ ��
��3��������������Һ����CO2 �� ѡ �� ��������Ϊ ��
��4��������ˮ��ȡ����ˮ��ѡ �� ��������Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com