
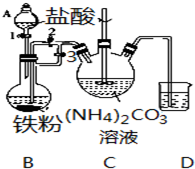
 ijС����̽��Cl2��KI��Һ�ķ�Ӧ�����ʵ��װ������ͼ��
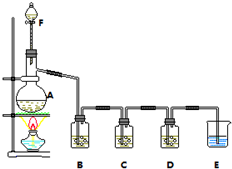
ijС����̽��Cl2��KI��Һ�ķ�Ӧ�����ʵ��װ������ͼ������ F�е�Ũ���������ƿA�еĶ��������з�����Ӧ�����������������̡�ˮ�����ɵ������к��Ȼ��⡢ˮ������ͨ��B�еı���ʳ��ˮ��ȥ�Ȼ��⣬ͨ��C��KI��Һ
��̽��Cl2��KI��Һ�ķ�Ӧ��ͨ��Dװ����AgNO3��Һ�����Ȼ�����ɫ���������ʣ������ͨ������������Һ���գ������ŷŵ������У���ֹ��Ⱦ������
��1��A�����Ʊ�������װ�ã�����A��������ƿ��B��������ȥ�����е��Ȼ������壻
��2��������KI��Һ��Ӧ֮��ʣ�������������������Һ��δ��Ӧ��������������������Һ�����գ�
��3�������ѵ����������ɵ��ʵ⣻���û�������I2��KI��Һ���ܽ�ȡ��ϴ�������Һ��ɫ��������ŷ�ӦKI�����ģ�ƽ��I2��S��+I-?I3-��aq�������ƶ�������ˮ�е��ܽ�Ƚ�С��
��4����������ʱ�Ὣ�����������HIO3��Na2S2O3�����ʵ���=0.625��0.024=0.015mol��C��ԭI-�����ʵ���=0.005��0.5=0.0025mol���豻��������Ϊx�ۣ��ݷ�ӦI2+2S2O32-��2I-+S4O62-���÷�Ӧ�ĵⵥ�����ʵ���=0.015��$\frac{1}{2}$=0.0075mol����ԭ�ӹ�0.015mol��x�۵����ɵ�ռ0.0025mol������������ɵ�Ϊ0.015-0.0025=0.0125mol���ݻ��ϼ�������ȼ��㣻
��5������ij��Һ���Ƿ���I-��ȡ�����μӵ�����Һ�����Ⱥ�����μ�����ˮ����
��� �⣺��1��A�����Ʊ�������װ�ã���������ͼ�κ���;��֪A��������ƿ��B����������ȥ�����е��Ȼ������壬�����ñ���ʳ��ˮ��
�ʴ�Ϊ��������ƿ������ʳ��ˮ��
��2��������KI��Һ��Ӧ֮��ʣ�������������������Һ��װ��D�������Ȼ�����ɫ������δ��Ӧ����������װ��E�е�����������Һ�����գ�
�ʴ�Ϊ����ɫ����������δ��Ӧ��������
��3��������ʼ����Cʱ���������������ɵ��ʵ⣬���Կ�ʼ��Һ���ػ�ɫ��������C��ͨ��������������Һ��ɫ��������������ɫ��������Ϊ���û�������I2��KI��Һ���ܽ�ȡ��ϴ�������Һ��ɫ��������ŷ�ӦKI�����ģ�ƽ��I2��S��+I-?I3-��aq�������ƶ�������ˮ�е��ܽ�Ƚ�С�����Բ��ֵ��Գ�������ʽ������
�ʴ�Ϊ����Һ���ػ�ɫ�����û�������I2��KI��Һ���ܽ�ȡ��ϴ�������Һ��ɫ��������ŷ�ӦKI�����ģ�ƽ��I2��S��+I-?I3-��aq�������ƶ�������ˮ�е��ܽ�Ƚ�С�����Բ��ֵ��Գ�������ʽ������
��4����������ʱ�Ὣ�����������HIO3��Na2S2O3�����ʵ���=0.625��0.024=0.015mol��C��ԭI-�����ʵ���=0.005��0.5=0.0025mol��
�豻��������Ϊx�ۣ��ݷ�ӦI2+2S2O32-��2I-+S4O62-���÷�Ӧ�ĵⵥ�����ʵ���=0.015mol��$\frac{1}{2}$=0.0075mol����ԭ�ӹ�0.015mol��
x�۵����ɵ�ռ0.0025mol������������ɵ�Ϊ0.015-0.0025=0.0125mol��
�ݻ��ϼ�������ȵã�0.0025x=0.0125��x=5��
���Ե�Ԫ�صĻ��ϼ�Ϊ+5�ۣ�
�ʴ�Ϊ��HIO3��+5��
��5������ij��Һ���Ƿ���I-��ȡ�����μӵ�����Һ�����Ⱥ�����μ�����ˮ����
�ʴ�Ϊ��ȡ���μӵ�����Һ�����Ⱥ�����μ�����ˮ����
���� ���⿼�����������ʵ�ʵ����ơ��������Ʊ������ʡ�������ԭ��Ӧ����Ŀ�Ѷ��еȣ�ע�⺬�������е�Ԫ�صĻ��ϼ۵�ȷ���ͼ��㣬��ȷ���ʵ����ʼ������Ļ�ѧ��Ӧ�ǽ����Ĺؼ�������������ѧ���ķ�����������������ѧʵ��������


 ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ĸɱ� | B�� | ����ĺ�ˮ | C�� | ���µĿ��� | D�� | ��Ӳ�Ĵ���ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
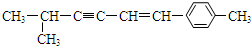 ������˵������ȷ���ǣ�������
������˵������ȷ���ǣ�������| A�� | �÷��������е�̼ԭ�Ӿ����ܴ���ͬһƽ���� | |
| B�� | �÷�����һ�������̼ԭ��������Ϊ8�� | |
| C�� | �÷�����������9��̼ԭ�Ӵ���ͬһ��ֱ���� | |
| D�� | �÷����п��ܹ����̼ԭ�������Ϊ13�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
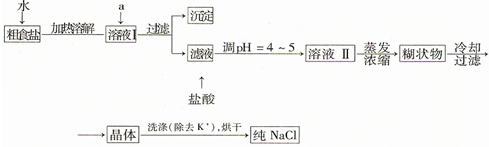
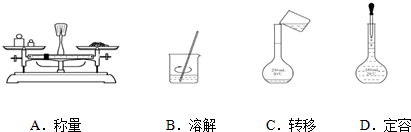
 ��������{[CH3CH��OH��COO]2Fe}��һ�ֺܺõ�ʳƷ��ǿ������������ˮ������Ч���������ã�����������FeCO3��Ӧ�Ƶã�
��������{[CH3CH��OH��COO]2Fe}��һ�ֺܺõ�ʳƷ��ǿ������������ˮ������Ч���������ã�����������FeCO3��Ӧ�Ƶã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
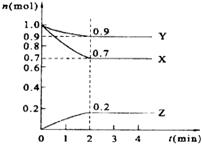 ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ��
ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
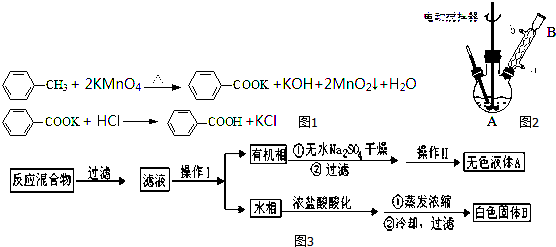
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ʵ������NaBr��ŨH2SO4���Ҵ�Ϊԭ�ϣ��Ʊ������飬��Ӧ�Ļ�ѧ����ʽΪ��
ʵ������NaBr��ŨH2SO4���Ҵ�Ϊԭ�ϣ��Ʊ������飬��Ӧ�Ļ�ѧ����ʽΪ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com