
【题目】对于密闭容器中的可逆反应:mX(g)+nY(s) ![]() pZ(g) ΔH<0,达到平衡后,改变条件,下列表述不正确的是
pZ(g) ΔH<0,达到平衡后,改变条件,下列表述不正确的是
A.增大压强,化学平衡不一定发生移动
B.通入氦气,化学平衡不一定发生移动
C.增加X或Y的物质的量,化学平衡一定发生移动
D.其他条件不变,升高温度,化学平衡一定发生移动
【答案】C
【解析】由于该反应体积变化不明确,故改变压强不能确定化学平衡是否移动,A项正确;在恒容条件下充入氦气,没有改变平衡体系中各物质的浓度,平衡不移动,B项正确;由于Y为固体,改变其用量不影响化学平衡,C项不正确;对于任何反应只要改变温度,平衡状态均改变,D项正确。
所以答案是:C
【考点精析】通过灵活运用化学平衡状态本质及特征和化学平衡移动原理以及影响因素,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);影响因素:①浓度:增大反应物(或减小生成物)浓度,平衡向正反应方向移动;②压强:增大压强平衡向气体体积减小的方向移动.减小压强平衡向气体体积增大的方向移动;③温度:升高温度,平衡向吸热反应方向移动.降低温度,平衡向放热反应方向移动;④催化剂:不能影响平衡移动即可以解答此题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有“锂”走遍天下。氧化锂(Li2O)是锂电池工业的重要原料,以粗碳酸锂为原料制备氧化锂的一种工艺流程如下:
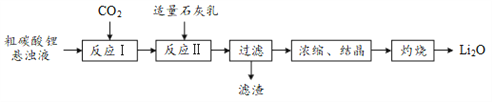
注:常温下,碳酸锂微溶于水,氢氧化锂可溶于水。
(1)反应Ⅰ中通入CO2需加压的原因是______。
(2)反应Ⅱ生成LiOH的化学方程式为______。
(3)浓缩、结晶所得LiOH·H2O通过灼烧得到Li2O。LiOH·H2O中常含有少量的Li2CO3,但该物质对所制Li2O的纯度无影响,其原因是______。
(4)锂离子电池大量应用在手机、笔记本电脑和家用小电器上。标记为Li-ion的锂离子电池的电池反应可表示为:Li + 2Li0.35NiO2![]() 2Li0.85NiO2。
2Li0.85NiO2。
①放电时,负极的电极反应式为______。
②充电时,能量转化形式主要是______。
③锂离子电池使用非水溶液做离子导体的原因是______(用离子方程式表示)。
④安全使用锂离子电池的措施有______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是

A. 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B. 当V=5时:c(CO32—)+c(HCO3-)+c(H2CO3)=c(Cl-)
C. 当V=10时:c(Na+)>c(HCO3-)>c(CO32—)>c(H2CO3)
D. 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种物质中 ①Ne ②H2O ③NH3④KOH ⑤Na2O(填写序号):只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法正确的是
![]() 原子间的相互吸引力叫做化学键
原子间的相互吸引力叫做化学键![]() 两种非金属原子间不可能形成离子键
两种非金属原子间不可能形成离子键![]() 强电解质的分子中一定存在离子键
强电解质的分子中一定存在离子键![]() 原子之间形成化学键的过程是能量降低的过程
原子之间形成化学键的过程是能量降低的过程![]() 所有的单质分子中都存在非极性共价键
所有的单质分子中都存在非极性共价键![]() 全部由非金属元素组成的化合物不一定是共价化合物( )
全部由非金属元素组成的化合物不一定是共价化合物( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年4月10日,陕西杨凌马拉松比赛中一参赛者在约41公里处突然倒地。少数运动员跑完全程时下肢肌肉会发生抽搐,这是由于随着大量排汗而向外排出了过量的( )
A.水 B.钙盐 C.钠盐 D.尿素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对物质性质的描述中属于离子晶体的是( )
A.熔点是1070℃,易溶于水,水溶液能导电
B.熔点是10.31℃,液态不导电,水溶液能导电
C.熔点3550℃,硬度大,不导电
D.熔点是97.80℃,质软、导电,密度是0.97g/cm3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com