
| A、在0℃,1.01×104Pa下,22.4L氯气与足量镁充分反应后,转移的电子数为2NA |
| B、常温常压下,14.9gKCl与NaClO的混合物中含氯元素的质量为7.1g |
| C、50mL 12mol?L-1浓盐酸与足量二氧化锰加热反应,生成Cl2分子的数目为1.15NA |
| D、某密闭容器中盛有0.2mol SO4和0.1molO2,在一定条件下充分反应,转移电子的数目为0.4NA |
| 35.5 |
| 74.5 |


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
| A、+2,+3 |
| B、+3,+2 |
| C、+2,+2 |
| D、+3,+3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
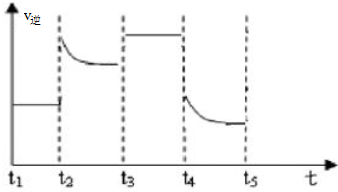
 如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )| A、①② | B、②④ | C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 点燃 |
| 点燃 |
| A、减小空气进量,增大天然气进量 |
| B、减小空气进量,减小天然气进量 |
| C、增大空气进量,增大天然气进量 |
| D、增大空气进量,减小天然气进量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙醇是生活中常见的有机物,能进行如图所示的多种反应,a、b、c、d都是含碳化合物.下列说法错误的是( )
乙醇是生活中常见的有机物,能进行如图所示的多种反应,a、b、c、d都是含碳化合物.下列说法错误的是( )| A、a的水溶液呈酸性 |
| B、反应②、④均为氧化反应 |
| C、c难溶于水 |
| D、可用金属钠区别乙醇和d |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯中的甲苯(溴水分液) |
| B、乙醇中的水(新制CaO蒸馏) |
| C、乙醛中的乙酸(NaOH蒸馏) |
| D、乙酸乙酯中的乙酸(饱和Na2CO3溶液分液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com