
【题目】通常状况下,CO是一种无色、无味、有毒的气体,难溶于水,与酸、碱、盐溶液均不反应。酒精喷灯可用作高温热源。正确连接如图所示的装置进行实验,可以验证某混合气体的成分是CO2和CO(每套装置限用一次)。请回答下列问题:
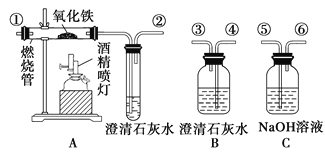
(1)连接装置导管口的顺序:混合气体→__________________→尾气处理(填导管接口代号)。
(2)证明原混合气体中CO2存在的实验现象是__________________________________;
证明CO存在的有关反应的化学方程式是__________________________________________。
(3)有同学提出仪器B应再使用一次,你认为有道理吗?________(填“有”或“没有”),并简述理由:
_________________________________________________________________。
(4)本实验尾气处理的方法是________________________________。
【答案】 ④③⑤⑥①② B中澄清石灰水不变浑浊,A中玻璃管粉末由红棕色变为黑色,试管中澄清石灰水变浑浊 Fe2O3+3CO![]() 2Fe+3CO2、Ca(OH)2+CO2=CaCO3↓+H2O 有 利用B→C→A不能说明二氧化碳在C中已经被除尽 在导管③后放置一个燃着的酒精灯(或用气囊收集)
2Fe+3CO2、Ca(OH)2+CO2=CaCO3↓+H2O 有 利用B→C→A不能说明二氧化碳在C中已经被除尽 在导管③后放置一个燃着的酒精灯(或用气囊收集)
【解析】(1)混合气体应先通入装置B检验CO2气体是否存在,气体应由长管④通入从短管③排出B装置;然后通入装置C,处理混合气体中的气体CO2,由⑤通入从⑥排出;接下来气体通入装置A,检验CO气体的存在,气体由①进入从②排出,所以连接导管口的顺序为:④③⑤⑥①②,故答案为:④③⑤⑥①②;
(2)若只有CO,B中澄请石灰水不变浑浊,A中玻璃管内粉末由红变黑,说明氧化铁被还原成铁,试管内澄清石灰水变浑浊,说明生成二氧化碳气体,两处现象综合,说明混合气体中只含有CO气体,反应的化学方程式有:Fe2O3+3CO![]() 2Fe+3CO2、Ca(OH)2+CO2=CaCO3↓+H2O,故答案为:B中澄清石灰水不变浑浊,A中玻璃管内粉末由红棕色变黑色,试管中澄清石灰水变浑浊;Fe2O3+3CO
2Fe+3CO2、Ca(OH)2+CO2=CaCO3↓+H2O,故答案为:B中澄清石灰水不变浑浊,A中玻璃管内粉末由红棕色变黑色,试管中澄清石灰水变浑浊;Fe2O3+3CO![]() 2Fe+3CO2、Ca(OH)2+CO2=CaCO3↓+H2O;
2Fe+3CO2、Ca(OH)2+CO2=CaCO3↓+H2O;
(3)由于利用B→C→A不能说明二氧化碳在C中已经被除尽,应该再使用一次仪器B证明二氧化碳气体已经除尽,故答案为:有;利用B→C→A不能说明二氧化碳在C中已经被除尽;
(4)尾气中含有有毒的CO气体,需要进行尾气处理,方法为:可在导管③后放置一个燃着的酒精灯或用气囊收集,故答案为:在导管③后放置一个燃着的酒精灯(或用气囊收集)。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】常温下,发生下列几种反应:①16H++10Z-+2XO![]() ===2X2++5Z2+8H2O ②2A2++B2===2A3++2B③2B-+Z2===B2+2Z-根据上述反应,判断下列结论错误的是
===2X2++5Z2+8H2O ②2A2++B2===2A3++2B③2B-+Z2===B2+2Z-根据上述反应,判断下列结论错误的是
A. 溶液中可发生:Z2+2A2+===2A3++2Z-
B. 氧化性强弱的顺序为:XO![]() >Z2>B2>A3+
>Z2>B2>A3+
C. Z2在①③反应中为还原剂
D. X2+是XO![]() 的还原产物
的还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可采用惰性电极处理含Na2SO4的废水,得到其它工业产品。其原理如图所示,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

下列叙述不正确的是
A. 通电后中间隔室的SO42-离子向正极区迁移,电解后正极区PH减小
B. ab为阳离子交换膜,负极区得到NaOH溶液
C. 负极区反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D. 每有1molO2生成,会有4molNa+进入负极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1996年2月,德国某研究所在高能加速器中,将70Zn 撞入一个208Pb的原子核并释放出一个中子后,合成一种人造超重元素的原子。该元素原子内中子数为( )
A. 278 B. 277 C. 166 D. 165
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ、(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:____________与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?_________;说明理由:___________。
Ⅱ、利用下图装置可以验证非金属性的变化规律。

(3)仪器A的名称为________,干燥管D的作用是_____________________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、_______、______,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为____________________________。
(5)已知C中是硅酸钠溶液,如要证明非金属性:C > Si,请选择相应的试剂,则A中加________、B中加________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产生活中有着重要的应用。请按要求写出相应的方程式。
(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO2-4,其总反应为2SO2+O2+2H2O=2H2SO4。上述总反应分两步进行,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,写出第二步反应的离子方程式: 。
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液。若溶液的pH偏高,则碱式硫酸铝产率降低且有气泡产生,用化学方程式表示其原因: 。
(3)ClO2是一种高效安全的杀菌消毒剂。氯化钠电解法生产ClO2工艺原理示意图如下:

①写出氯化钠电解槽内发生反应的离子方程式: 。
②写出ClO2发生器中的化学方程式,并标出电子转移的方向及数目: 。
③ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,自身被还原成Cl-。写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.碳酸钠可用于去除餐具的油污B.碳酸钡可用于胃肠X射线造影检查
C.氢氧化铝可用于中和过多胃酸D.漂白粉可用于生活用水的消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 按系统命名法,化合物![]() 的名称为2-乙基丙烷
的名称为2-乙基丙烷
B. 丙烯分子中,最多有7个原子共面
C. 蔗糖和淀粉的水解产物相同且均为葡萄糖
D. 向鸡蛋清中加入Pb(CH3COO)2或(NH4)2SO4溶液均会产生沉淀,两者的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、科学、技术、社会、环境密切相关,下列说法中不正确的是
A. 硅单质可作为制造宇宙飞船太阳能电池帆板的主要材料
B. 硫酸铜溶液可用来浸泡蔬菜,以保持蔬菜的新鲜
C. 常用明矾、硫酸铁等物质来处理污水中的悬浮物质
D. 提倡使用共享单车,目的是为了降低碳排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com