
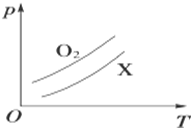
 如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )
如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体不可能是( )| A. | C2H6 | B. | CH4 | C. | CO2 | D. | SO2 |
科目:高中化学 来源: 题型:选择题
| A. | 在AsCl3分子构型为三角锥形 | |
| B. | Na3AsO4溶液的pH大于7 | |
| C. | 砷的氢化物的化学式为AsH3,它的沸点比NH3低 | |
| D. | 砷元素的相对原子质量为75,由此可知砷原子核内必有42个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA | |
| B. | 电解精炼铜时,阴极质量增加12.8g时,转移电子0.4NA | |
| C. | 标准状况下,2.24LCH2Cl2含有分子的数目为0.1NA | |
| D. | 常温常压下,将0.1mol Fe投入足量的浓硝酸中,转移的电子为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 | |
| B. | NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 | |
| C. | pH值相等的三种溶液:①NH4Cl ②(NH4)2SO4③NH4HSO4中c(NH4+)大小顺序为②>①>③ | |
| D. | 加热0.1 mol•L-1 Na2CO3溶液,CO32-的水解程度和溶液的pH均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.6gNO2气体约含有1.81×1023个原子 | |
| B. | 在标准状况下,80gSO3所占的体积约为22.4L | |
| C. | 常温下,IL0.lmol/L磷酸溶液含有0.1NA个H+ | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质熔点、沸点逐渐降低 | B. | 单质的氧化性逐渐增强 | ||
| C. | 元素的非金属性递减 | D. | 气态氢化物稳定性递增 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com