
Ź¢ÓŠ12 mL NO2ŗĶO2µÄ»ģŗĻĘųĢåµÄĮæĶ²µ¹Į¢ÓŚĖ®²ŪÖŠ£¬³ä·Ö·“Ó¦ŗó£¬ »¹Ź£Óą2 mLĪŽÉ«ĘųĢ壬ŌņŌ»ģŗĻĘųĢåÖŠO2µÄĢå»żŹĒ (””””)
»¹Ź£Óą2 mLĪŽÉ«ĘųĢ壬ŌņŌ»ģŗĻĘųĢåÖŠO2µÄĢå»żŹĒ (””””)
A£®1.2 mL  B£®2.4 mL
B£®2.4 mL
C£®3.6 mL D£®4.8 mL

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
A£®ĮņŹĒŅ»ÖÖµ»ĘÉ«µÄ²»ČÜÓŚĖ®µÄ¾§Ģå
B£®ĮņµÄ»ÆŗĻĪļ³£“ęŌŚÓŚ»šÉ½Åē·¢µÄĘųĢåÖŠŗĶæóČŖĖ®ÖŠ
C£®µ„Š±ĮņŗĶŠ±·½Įņ¶¼ŹĒĮņµ„ÖŹ
D£®ĮņŌŚæÕĘųÖŠČ¼ÉյIJśĪļŹĒSO2£¬ŌŚ“æŃõÖŠµÄČ¼ÉÕ²śĪļŹĒSO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øł¾ŻĻĀĮŠ»Æѧ·“Ó¦ŗĶŹĀŹµ£¬ĖµĆ÷·“Ó¦ĄūÓĆĮĖĮņĖįµÄŹ²Ć“ŠŌÖŹ£¬½«±ķŹ¾ŠŌÖŹµÄŃ”ĻīµÄ×ÖÄøĢīŌŚø÷Š”ĢāµÄŗįĻßÉĻ”£
A£®²»»Ó·¢ŠŌ”””””””””” B£®ĖįŠŌ
C£®ĪüĖ®ŠŌ D£®ĶŃĖ®ŠŌ
E£®ĒæŃõ»ÆŠŌ F£®ĒæĖįŠŌ
£Ø1£©ÅØĮņĖįæÉ×÷ĘųĢåøÉŌļ¼Į________£»
£Ø2£©ÕįĢĒÖŠ¼ÓÅØH2SO4²śÉś”°ŗŚĆę°ü”±ĻÖĻó________£»
£Ø3£©2NaCl£«H2SO4(ÅØ)Na2SO4£«2HCl”ü________£»
£Ø4£©Zn£«H2SO4(Ļ”)===ZnSO4£«H2”ü________£»
£Ø5£©Na2SO3£«H2SO4(Ļ”)===Na2SO4£«SO2”ü£«H2O________£»
£Ø6£©Cu£«2H2SO4(ÅØ)CuSO4£«SO2”ü£«2H2O________£»
(7)C£«2H2SO4(ÅØ)2SO2”ü£«2H2O£«CO2”ü________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹ŲĪļÖŹµÄŠŌÖŹÓėÓ¦ÓĆ²»Ļą¶ŌÓ¦µÄŹĒ””(””””)
A£®Ć÷·ÆÄÜĖ®½āÉś³ÉAl(OH)3½ŗĢ壬æÉÓĆ×÷¾»Ė®¼Į
B£®FeCl3ČÜŅŗÄÜÓėCu ·“Ó¦£¬æÉÓĆÓŚŹ“æĢÓ”Ė¢µēĀ·
C£®SO2¾ßÓŠŃõ»ÆŠŌ£¬æÉÓĆÓŚĘÆ°×Ö½½¬
D£®Zn¾ßÓŠ»¹ŌŠŌŗĶµ¼µēŠŌ£¬æÉÓĆ×÷ŠæĆĢøɵē³ŲµÄøŗ¼«²ÄĮĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
°ŃÉŁĮæNO2ĘųĢåĶØČė¹żĮ抔ĖÕ“ņČÜŅŗÖŠ£¬ŌŁŹ¹ŅŻ³öµÄĘųĢåĶعż×°ÓŠ×ćĮæµÄ¹żŃõ»ÆÄĘæÅĮ£µÄøÉŌļ¹Ü£¬×īŗóŹÕ¼Æµ½µÄĘųĢåŹĒ (””””)
A£®ŃõĘų B.¶žŃõ»ÆµŖ
C£®¶žŃõ»ÆµŖŗĶŃõĘų D£®¶žŃõ»ÆµŖŗĶŅ»Ńõ»ÆµŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĶ¼ŹĒ֊ѧ»Æѧ֊³£¼ūĪļÖŹ¼äµÄ·“Ó¦×Ŗ»Æ¹ŲĻµĶ¼£¬ĘäÖŠ²æ·Ö²śĪļŅŃĀŌČ„£®³£ĪĀĻĀ£¬GĪŖ¹ĢĢåµ„ÖŹ£¬B”¢IĪŖŅŗĢ壬ĘäÓą¶¼ĪŖĘųĢ壮AĪŖ»ÆŗĻĪļ£¬IµÄÅØČÜŅŗÓėGŌŚ¼ÓČČĢõ¼žĻĀÉś³ÉF”¢BŗĶC.HæÉÓĆ×÷¹¤ŅµÉĻŅ±Į¶½šŹōµÄ»¹Ō¼Į£®Ēė°“ŅŖĒóĢīæÕ£ŗ
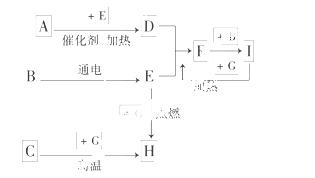
£Ø1£©Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗ
A£ŗ________£»B£ŗ________£»C£ŗ________.
£Ø2£©Š“³öF£«B”Ŗ”śIµÄ»Æѧ·½³ĢŹ½____________________________________£®
£Ø3£©Š“³öGŗĶIµÄÅØČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½________________________________
____________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹¤Ņµ³£ÓĆČ¼ĮĻÓėĖ®ÕōĘų·“Ó¦ÖʱøH2ŗĶCO£¬ ŌŁÓĆH2ŗĶCOŗĻ³É¼×“¼”£
£Ø1£©ÖĘČ”H2ŗĶCOĶس£²ÉÓĆ£ŗC(s)+H2O(g)  CO(g)+H2(g) ”÷H£½+131.4 kJ”¤mol-1£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ ”£
CO(g)+H2(g) ”÷H£½+131.4 kJ”¤mol-1£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ ”£
a£®øĆ·“Ó¦µÄ·“Ó¦Īļ×ÜÄÜĮæŠ”ÓŚÉś³ÉĪļ×ÜÄÜĮæ
b£®±ź×¼×“æöĻĀ£¬ÉĻŹö·“Ӧɜ³É1L H2ĘųĢåŹ±ĪüŹÕ131.4 kJµÄČČĮæ
c£®ČōCO(g)+H2(g) C(s)+H2O(1) ”÷H£½£QkJ”¤mol-1£¬ŌņQ£¼131.4
C(s)+H2O(1) ”÷H£½£QkJ”¤mol-1£¬ŌņQ£¼131.4
d£®ČōC(s)+CO2(g) 2CO(g) ”÷H1£»CO(g)+H2O(g)
2CO(g) ”÷H1£»CO(g)+H2O(g) H2(g)+CO2(g) ”÷H2 Ōņ£ŗ”÷H1+”÷H2£½+131.4 kJ”¤mol-1
H2(g)+CO2(g) ”÷H2 Ōņ£ŗ”÷H1+”÷H2£½+131.4 kJ”¤mol-1
£Ø2£©¼×ĶéÓėĖ®ÕōĘų·“Ó¦Ņ²æÉŅŌÉś³ÉH2ŗĶCO£¬øĆ·“Ó¦ĪŖ£ŗCH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
ŅŃÖŖŌŚÄ³ĪĀ¶ČĻĀ2LµÄĆܱվųČČČŻĘ÷ÖŠ³äČė2.00mol¼×ĶéŗĶ1.00molĖ®ÕōĘų£¬²āµĆµÄŹż¾ŻČēĻĀ±ķ£ŗ
| ²»Ķ¬Ź±¼äø÷ĪļÖŹµÄĪļÖŹµÄĮæ/mol | ||||
| 0 min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |
øł¾Ż±ķÖŠŹż¾Ż¼ĘĖć£ŗ
¢Ł0 min ~ 2min ÄŚH2µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ ”£
¢Ś“ļĘ½ŗāŹ±£¬ CH4µÄ×Ŗ»ÆĀŹĪŖ ”£ŌŚÉĻŹöĘ½ŗāĢåĻµÖŠŌŁ³äČė2.00mol¼×ĶéŗĶ1.00mol Ė®ÕōĘų£¬“ļµ½ŠĀĘ½ŗāŹ±H2µÄĢå»ż·ÖŹżÓėŌĘ½ŗāĻą±Č £ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©£¬æÉÅŠ¶ĻøĆ·“Ó¦“ļµ½ŠĀĘ½ŗāדĢ¬µÄ±źÖ¾ÓŠ______”££ØĢī×ÖÄø£©
a£®COµÄŗ¬Įæ±£³Ö²»±ä b£®ČŻĘ÷ÖŠc(CH4)Óėc(CO)ĻąµČ
c£®ČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä d£®3¦ĶÕż£ØCH4£©=¦ĶÄę£ØH2£©
£Ø3£©ŗĻ³É¼×“¼¹¤³§µÄĖįŠŌ·ĻĖ®ÖŠŗ¬ÓŠ¼×“¼£ØCH3OH£©£¬³£ÓĆĻņ·ĻŅŗÖŠ¼ÓČėĮņĖįīÜ£¬ŌŁÓĆĪ¢ÉśĪļµē³Ųµē½ā£¬µē½āŹ±Co2+±»Ńõ»Æ³ÉCo3+£¬Co3+°ŃĖ®ÖŠµÄ¼×“¼Ńõ»Æ³ÉCO2£¬“ļµ½³żČ„¼×“¼µÄÄæµÄ”£¹¤×÷ŌĄķČēĻĀĶ¼£Ø cĪŖøōĤ£¬¼×“¼²»ÄÜĶعż£¬ĘäĖüĄė×ÓŗĶĖ®æÉŅŌ×ŌÓÉĶعż£©”£
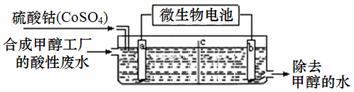
¢Łaµē¼«µÄĆū³ĘĪŖ ”£
¢ŚŠ“³ö³żČ„¼×“¼µÄĄė×Ó·½³ĢŹ½ ”£
¢ŪĪ¢ÉśĪļµē³ŲŹĒĀĢÉ«ĖįŠŌČ¼ĮĻµē³Ų£¬Š“³öøƵē³ŲÕż¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÖŠŃėµēŹÓĢØŌų±ØµĄ¼ĶĮŖ»Ŗ³¬ŹŠŌŚŹŪµÄÄ³Ę·ÅĘ¼¦µ°ĪŖ”°ĻšĘ¤µÆ”±£¬ ÖóŹģŗóµ°»ĘČĶŠŌŹ¤¹żĘ¹ÅŅĒņ£¬µ«¾¼ģ²āĪŖÕę¼¦µ°”£×ؼŅ½éÉÜ£¬ÕāŹĒÓÉÓŚ¼¦ĖĒĮĻĄļĢķ¼ÓĮĖĆŽ×ѱż£¬“Ó¶ųŹ¹¼¦µ°Ąļŗ¬ÓŠ¹ż¶ąĆŽ·ÓĖłÖĀ”£Ęä½į¹¹¼ņŹ½ČēÓŅĶ¼ĖłŹ¾£ŗĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
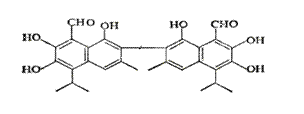
A”¢øĆ»ÆŗĻĪļµÄ·Ö×ÓŹ½ĪŖ£ŗC30H30O8
B”¢1molĆŽ·Ó×ī¶ąæÉÓė10mol H2¼Ó³É£¬Óė6molNaOH·“Ó¦
C”¢ŌŚŅ»¶ØĢõ¼žĻĀ£¬æÉÓėŅŅĖį·“Ӧɜ³Éõ„ĄąĪļÖŹ
D”¢øĆĪļÖŹæÉŅŌŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com