
����һ����Ҫ�Ļ�����Ʒ���ǵ��ʹ�ҵ���л��ϳɹ�ҵ�Լ��������ᡢ��κʹ���ȵ�ԭ�ϡ�
��1����Ϊȼ�Ͽ���������찱ȼ�ϵ�أ����������Ⱦ���ںܶ�����õ��㷺Ӧ�á����缫���Ͼ�Ϊ���Ե缫��KOH��Һ���������Һ����õ�ظ����缫��ӦʽΪ ��
��2����һ���¶��£��ڹ̶�������ܱ������н��п��淴Ӧ��N2+3H2 2NH3���ÿ��淴Ӧ�ﵽƽ��ı�־��________________��
2NH3���ÿ��淴Ӧ�ﵽƽ��ı�־��________________��
A��3v(H2)��=2v(NH3)��
B����λʱ������m mol N2��ͬʱ����3m mol H2
C�������ڵ���ѹǿ������ʱ����仯
D�����������ܶȲ�����ʱ��仯
E��a molN��N�����ѵ�ͬʱ����6amolN—H������
F��N2��H2��NH3�ķ�����֮��Ϊ1��3��2
��3��ij��ѧ�о���ѧϰС��ģ�ҵ�ϳɰ��ķ�Ӧ�����ݻ��̶�Ϊ2L���ܱ������ڳ���1molN2��3molH2��������ʴ�����������Ժ��Բ��ƣ�����һ���¶�ѹǿ�¿�ʼ��Ӧ������ѹ���Ƽ��������ѹǿ�ı仯���£�
| ��Ӧʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| ѹǿ/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
��ӷ�Ӧ��ʼ��25minʱ����N2��ʾ��ƽ����Ӧ����= �����¶���ƽ�ⳣ��K= ��
��4����CO2��NH3Ϊԭ�Ϻϳ�����[��ѧʽΪCO(NH2)2]����Ҫ��Ӧ���£���֪��
��2NH3(g)+CO2(g) == NH2CO2 NH4(s) ��H= —l59.5 kJ·mol-1
��NH2CO2NH4(s)  CO(NH2)2(s)+H2O(g) ��H=+116.5 kJ·mol-1
CO(NH2)2(s)+H2O(g) ��H=+116.5 kJ·mol-1
��H2O(1) == H2O(g) ��H=+44.0kJ·mol-1
д��CO2��NH3�ϳ����غ�Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽ ��
����������Ӧ�����ܱ������н�����NH2CO2NH4������300K�·ֽ⣬ƽ��ʱP[H2O(g)]Ϊa Pa������Ӧ�¶Ȳ��䣬����ϵ���������50%����P[H2O(g)]��ȡֵ��Χ��_________________���ú�a��ʽ�ӱ�ʾ��������ѹ=��ѹ�����ʵ���������
��֪ʶ�㡿��ѧƽ�� G1 G2 G3 G4 G5
���𰸽�����24����1��2NH3—6e—+6OH—=N2+6H2O 3��
��2��BCE 3��
��3��0.01 mol/(L.min) 2�� 2.37( mol/L)-2 2��
��4��2NH3(g)+CO2(g)== CO(NH2)2(s) +H2O(l) ��H= — 87.0 kJ·mol-1 2��
2a/3��P[H2O(g)]��a 2��
��������1��ȼ�ϵ��ȼ��Ϊ����������������Ӧ
��2��A������ʾ�����������ʣ���A����B����ȷ��C����Ӧ�����У���������仯ѹǿ�仯����һ������ﵽƽ�⣬C��ȷ��D��m���䣬V���䣬���ܶȲ��䣬����ƽ���־����D����E����ȷ��F��ƽ���־�Ǹ����Ũ�Ȳ��䣬��F����ѡ��BCE
��3����3��ʽ 2L ���ʵ���mol N2+3H2 2NH3
2NH3
��ʼ���ʵ���1 3 0
�仯�� x 3x 2x
ƽ���� 1-x 3-3x 2x
25min��0minѹǿ��Ϊ12.6/16.8=��4-2x��/4��x=0.5mol����N2��ʾ��ƽ����Ӧ����=0.5mol��2L��25min=0.01 mol/(L.min)��ƽ�ⳣ��K=c2��������/c3(����)��c��������= 2.37( mol/L)-2
��4��2NH3(g)+CO2(g)== CO(NH2)2(s) +H2O(l) ��H=—l59.5 kJ·mol-1+116.5 kJ·mol-1-44.0kJ·mol-1= — 87.0 kJ·mol-1
��5������ϵ���������50%����P[H2O(g)]��Ϊ2a/3����ƽ���������ƶ���2a/3��P[H2O(g)]��a
��˼·�㲦���⿼����������ԭ��Ӧ����˹���ɡ���ѧƽ���֪ʶ�㣬����������ԭ��Ӧʵ�ʡ���˹�����ں�����ѧƽ����жϷ�����֪ʶ�������������Щ֪ʶ�㶼�Ǹ߿��ȵ㣬���������ڴ����ۺ����У�ע�����غ�˼�����������⣬��Ŀ�Ѷ��еȣ�


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��CO�ϳɼ״���CH3OH��
�Ļ�ѧ��Ӧ����ʽΪCO(g)+2H2(g) CH3OH(g) ����H��0
CH3OH(g) ����H��0
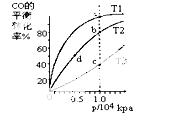
������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ������˵����
 ȷ����( )
ȷ����( )
A��ƽ�ⳣ����K(a)��K(c) K(b)��K(d)
B������Ӧ���ʣ�v(a)��v(c) v(b)��v(d)
C��ƽ��Ħ��������M(a)��M(c) M(b)��M(d)
D��ƽ��ʱa��һ����n(CO)��n(H2)��1:2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о�С��Ϊ̽���������������������绯ѧ��ʴ���͵�Ӱ�����أ�����Ͼ��ȵ��������ۺ�̼��������ƿ�ײ�������ƿ��(��ͼ1)���ӽ�ͷ�ι��е��뼸�δ�����Һ��ͬʱ���������е�ѹǿ�仯��
��1�����������ʵ����Ʊ�(���в�Ҫ���� ��)��
��)��
| ��� | ʵ��Ŀ�� | ̼��/g | ����/g | ����/% |
| �� | Ϊ����ʵ�������� | 0.5 | 2.0 | 90.0 |
| �� | ����Ũ�ȵ�Ӱ�� | 0.5 | 36.0 | |
| �� | 0.2 | 2.0 | 90.0 |
��2����Ţ�ʵ����������ѹǿ��ʱ��仯��ͼ2��t2ʱ��������ѹǿ����С����ʼѹǿ����ԭ������������ ��ʴ������ͼ3���ü�ͷ��������ø�ʴʱ������������ʱ��̼�۱��淢���� (����������ԭ��)��Ӧ����缫��Ӧʽ�� ��
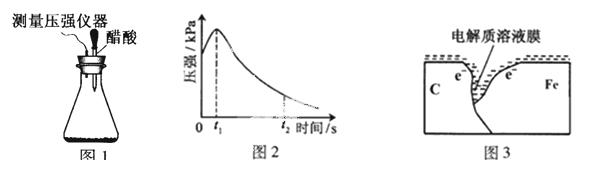
��3����С���ͼ2��0��t1ʱѹǿ����ԭ����������¼��裬������ɼ������
����һ���������ⸯʴ���������壻
�������  ��
��
����
��4��Ϊ��֤����һ��ijͬѧ����˼����ռ����������Ƿ���H2�ķ��������������һ��ʵ�鷽����֤����һ��д��ʵ�鲽��ͽ��ۡ�
| ʵ�鲽��ͽ���(��Ҫ��д�����������)�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ӫ���ḻ�����С��߲�֮����֮�ƣ���һ�ָ�Ч�IJ���������������������������˲����붹��ͬʳ���������˸��Ȳ��˾���Ҷ����Ӫ������˵����ijѧУ��ѧ��ȤС���ͬѧ��ͨ��ʵ��̽���������⣺
�ٲ����Ƿ��зḻ������
�ڲ����Ƿ��в��������ʣ�
�۲��˸������ĺ����Ƿ�Ȳ��˾���Ҷ�еĸߣ�
ͨ��������ѯ������������ϣ����������Ҷ��ᣬ�����Ա�������ǿ�����ἰ���ξ��н�ǿ�Ļ�ԭ�ԣ����в���Ʋ�����ˮ��
������Ƶ�ʵ�鲽�����£�
��.
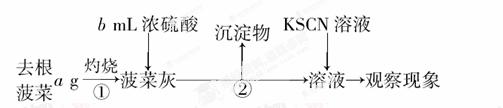
��.ȡ���˸�a g��ʹ����ͬ�������Լ����ظ�I��ʵ�飬�۲�ʵ������
��.��������������ˮ�����2��3 min����ȴ����ȥ���ˣ�����Һ������Һ�м�������Ca(OH)2��Һ��Ȼ���ټ��������Լ�X���۲�����
��ش��������⣺
(1)��������ʹ�õ����������żܡ��ƾ��ơ����������Ҫ________�������ڵ�������________��
(2)����˵�����˸���FeԪ�غ���Ҫ�Ȳ��˾���Ҷ�ж��������________��
(3)�����е�Fe�ǣ�2�ۻ��ǣ�3�ۣ�________��
(4)ͨ����������ȷ�������к��в��������ʡ�������Һ�к���CO32������������Լ�X�ų�CO32���ĸ��š���X��________(д��ѧʽ)�������Լ�X��۲쵽��������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijУ��ѧ�о���ѧϰС����ѧϰ�˽�����֪ʶ��̽��Cu�ij�������������ʡ��������£�
������⣺
�������ڱ��У�Cu��Alλ�ýӽ���Cu����Al���ã�Al(OH)3�������ԣ�Cu(OH)2Ҳ����������
��ͨ������£�Fe2�����ȶ���С��Fe3���ģ�Cu�����ȶ���ҲС��Cu2������
��CuO�������ԣ��ܱ�H2��CO�Ȼ�ԭ��Ҳ�ܱ�NH3��ԭ��
ʵ�鷽����
(1)�����������õ���ҩƷ��CuSO4��Һ��________(���Լ�����)��ͬʱ�������ʵ�顣
(2)�������ڵ�ʵ�鲽����������£�ȡ98 g Cu(OH)2���壬������80��100��ʱ���õ� 80 g��ɫ�����ĩ���������ȵ�1  000�����ϣ���ɫ��ĩȫ����ɺ�ɫ��ĩA����ȴ�������A������Ϊ72 g��A�Ļ�ѧʽΪ________����A�м���������ϡ���ᣬ�õ���ɫ��Һ��ͬʱ�۲쵽�����л��к�ɫ������ڣ���Ӧ�����ӷ���ʽΪ___________________��
000�����ϣ���ɫ��ĩȫ����ɺ�ɫ��ĩA����ȴ�������A������Ϊ72 g��A�Ļ�ѧʽΪ________����A�м���������ϡ���ᣬ�õ���ɫ��Һ��ͬʱ�۲쵽�����л��к�ɫ������ڣ���Ӧ�����ӷ���ʽΪ___________________��
(3)Ϊ�������ۣ���Ƶ�ʵ��װ����ͼ��ʾ(�гּ�β������װ��δ����)��ʵ���й۲쵽CuO��Ϊ��ɫ���ʡ������Ͽ�֪��ͬʱ����һ������Ⱦ�����壬������Ļ�ѧʽΪ
__________________________________________________��
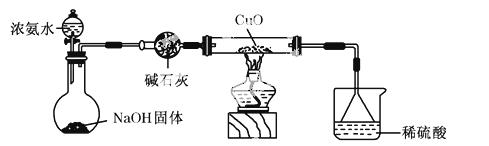
ʵ����ۣ�
(4)Cu(OH)2�������ԡ�֤��Cu(OH)2�������Ե�ʵ��������_____________________��
(5)����ʵ�鷽��(2)���ó���Cu����Cu2���ȶ��Դ�С�Ľ��ۣ�����ʱ________����������Һ��________��
(6)CuO�ܱ�NH3��ԭ��
�������ۣ�
��ͬѧ��ΪNH3��CuO��Ӧ�����ɵĺ�ɫ������Cu��Ҳ��ͬѧ��ΪNH3��CuO��Ӧ�����ɵĺ�ɫ������Cu��A�Ļ����������һ����ʵ�鷽����֤NH3��CuO��Ӧ�����ɵĺ�ɫ�������Ƿ���A��__________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�ܱ������г���һ������N2��O2���ڵ�������·�����ӦN2��O2===2NO�����ⶨǰ3 s��N2��ʾ�ķ�Ӧ����Ϊ0.1 mol·L��1·s��1����6 sĩNO��Ũ��Ϊ
A��1.2 mol·L��1 B������1.2 mol·L��1
C��С��1.2 mol·L��1 D������ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ�������´��ڷ�Ӧ��2SO2(g)��O2(g) 2SO3(g)����H��0���������������ͬ���ܱ�����I��II��III��������ͼ��ʾͶ�ϣ�����400�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ���� �� ��
2SO3(g)����H��0���������������ͬ���ܱ�����I��II��III��������ͼ��ʾͶ�ϣ�����400�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ���� �� ��
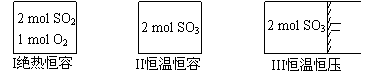

A������I��III��ƽ�ⳣ����ͬ
B������II��III������Ӧ������ͬ
C��SO3�����������II��III
D������I��SO2��ת����������II��SO3��ת����֮��С��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�����������˵����ȷ����
A���ú�0.1mol FeCl3����Һ��������ˮ��Ӧ�Ƶõ�Fe(OH)3�����н�����Ϊ0.1NA
B��46g NO2��N2O4�Ļ�������к�Nԭ������ΪNA
C����״���£�5.6L CCl4���еķ�����Ϊ0.25NA
D�������ʵ�����NH4����OH������������Ϊ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڷ�Ӧ:CaCO3��2HCl===CaCl2��H2O��CO2��������˵����ȷ����(����)
A����HCl��CaCl2��ʾ�ķ�Ӧ�������ݲ�ͬ��������ʾ��������ͬ
B��������CaCO3��Ũ�ȱ仯����ʾ��Ӧ���ʣ�������ˮ����ʾ
C����H2O��CO2��ʾ�Ļ�ѧ��Ӧ������ͬ
D��������CaCl2Ũ�ȵļ�С��ʾ�䷴Ӧ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com