
【题目】在体积为2 L的密闭容器中,充入6mol N2,10mol H2,发生反应:N2(g)+3 H2(g) ![]() 2NH3(g)反应进行5 min时,测得NH3的浓度为1mol·L-1,在此时间内,下列反应速率表示正确的是
2NH3(g)反应进行5 min时,测得NH3的浓度为1mol·L-1,在此时间内,下列反应速率表示正确的是
A.v(NH3)=0.1mol·L-1·min-1 B.v(H2)=0.7 mol·L-1·min-1
C.v(NH3)=0.2mol·L-1·min-1 D.v(H2)=0.5mol·L-1·min-1
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
【题目】
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 .
②某学生设计回收四氯化碳的操作为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体;
d.将分液漏斗充分振荡后静置
其中分液漏斗使用前须进行的操作是 ,上述操作正确的顺序是 (填序号)
(3)已知:I2+2S2O32﹣═2I﹣+S4O62﹣.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10﹣3mol· L﹣1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示) mg/kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,错误的是( )
A. 元素周期表中,有18个纵行即有18个族
B. 最外层电子数为2的元素原子,不一定属于ⅡA族元素
C. 在周期表里,元素所在的周期序数等于原子核外的电子层数
D. 副族与Ⅷ族元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学变化一定存在:①状态和颜色的变化 ②发光放热 ③生成新物质 ④气体的放出 ⑤能量的变化( )
A. ③ B. ③⑤ C. ②④⑤ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A. 3517Cl2与3717Cl2氧化能力相近,二者互为同位素
B. 过氧化氢的电子式:![]()
C. 同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱
D. 同周期主族元素原子半径随核电荷数的增大而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A.Fe、Fe2O3都能与稀盐酸反应,都属于置换反应
B.CaO、NaOH固体都能与水反应,都能作干燥剂
C.浓盐酸、浓硫酸都有挥发性,敞口放置浓度都会变小
D.NH4Cl、(NH4)2SO4都含有NH4+,都能与熟石灰反应生成NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )
A.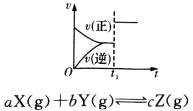 B.
B.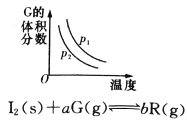
C.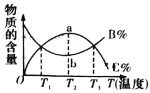 D.
D.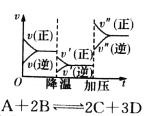
A.t0时改变某一条件有如图所示,则改变的条件一定是加入催化剂
B.反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应
C.从加入反应物开始,物质的百分含量与温度关系如图所示,则该反应的正反应为吸热反应
D.反应速率和反应条件变化如图所示,则该反应正反应为放热反应,A、B、C是气体、D为固体或液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是( )
A.由2H和18O所组成的水22g,其中所含的中子数为12 NA
B.分子数为NA的N2、CO混合气体体积在标况下为22.4 L,质量为28 g
C.标准状况下,22.4LNO和11.2L O2混合后气体的分子总数为NA
D.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com