
| A. | ①②⑥ | B. | ②③④ | C. | ②④⑥ | D. | ②④ |
分析 ①二氧化硅与氢氧化钠反应生成硅酸钠;
②S与氧气反应生成SO2;
③NH3与氯气反应生成N2;
④CuO不溶于水也不与水反应;
⑤Cl2与氢氧化钠反应生成次氯酸钠;
⑥二氧化硫在溶液中可以被氧化剂氧化为硫酸;
解答 解:①SiO2→Na2SiO3,二氧化硅是酸性氧化物,与碱反应生成盐和水,加入氢氧化钠溶液能一步实现,故①不选;
②S→SO3,S与氧气反应生成SO2,SO2再经氧化才生成SO3,因此不能通过一步反应实现,故②选;
③NH3与氯气反应生成N2,可以通过一步转化实现,故③不选;
④CuO不溶于水也不与水反应,所以氧化铜不能一步转化为氢氧化铜,故④选;
⑤Cl2与氢氧化钠反应生成次氯酸钠,可以实现一步转化,故⑤不选;
⑥二氧化硫在溶液中可以被氧化剂氧化为硫酸,如二氧化硫通入氯水中发生氧化还原反应生成硫酸,故⑥不选;
故选D.
点评 本题考查考查化学方程式的书写,涉及内容较多,明确物质间的转化关系是解题的关键,题目难度不大.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 56g铁片与足量浓H2SO4在加热的条件下可生成1.5NA个SO2分子 | |
| B. | 标准状况下20g D2O分子中所含中子数为10NA | |
| C. | 常温下,将0.1NA个氯化氢分子溶于1L水中,得到0.1mol/L的盐酸 | |
| D. | 2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨是离子化合物 | B. | 液氨是共价化合物 | ||
| C. | 液氨分子中含离子键 | D. | 一个液氨分子中含有7个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
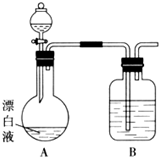 实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.
实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
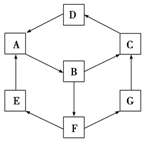 如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.
如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.| 物质 | 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
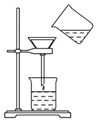 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
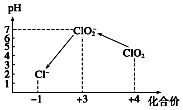 ClO2是一种黄绿色到橙黄色的气体,ClO2与Cl2的氧化性相近,被国际上公认为安全、低毒的绿色消毒剂,近几年我国用ClO2代替氯气对饮用水进行消毒.
ClO2是一种黄绿色到橙黄色的气体,ClO2与Cl2的氧化性相近,被国际上公认为安全、低毒的绿色消毒剂,近几年我国用ClO2代替氯气对饮用水进行消毒.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com