
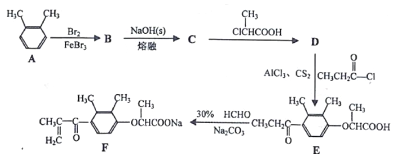
【题目】化合物F是一种药物合成的中间体,F的一种合成路线如下:

已知:

回答下列问题:
(1)![]() 的名称为____。
的名称为____。
(2)D中含氧官能团的名称为____。
(3)B→C的反应方程式为____。
(4)D→E的反应类型为____。
(5)C的同分异构体有多种,其中苯环上连有—ONa、2个—CH3的同分异构体还有____种,写出核磁共振氢谱为3组峰,峰面积之比为6:2:1的同分异构体的结构简式____。
(6)依他尼酸钠( )是一种高效利尿药物,参考以上合成路线中的相关信息,设计以
)是一种高效利尿药物,参考以上合成路线中的相关信息,设计以![]() 为原料(其他原料自选)合成依他尼酸钠的合成路线。________________
为原料(其他原料自选)合成依他尼酸钠的合成路线。________________
【答案】2-氯丙酸 羧基、醚键 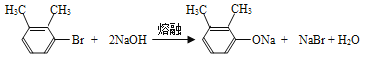 取代反应 5
取代反应 5 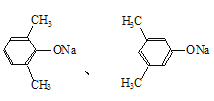
【解析】
由流程图可知:A在催化剂作用下发生苯环上溴代反应生成B,B发生取代反应生成C,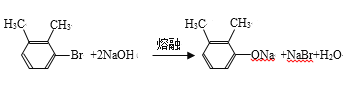 ,C发生信息中取代反应生成D,由信息D发生取代反应生成E,由E的结构、反应条件,逆推可知D为
,C发生信息中取代反应生成D,由信息D发生取代反应生成E,由E的结构、反应条件,逆推可知D为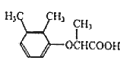 、C为
、C为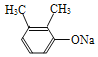 、B为
、B为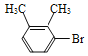 .对比E、F的结构,可知E的羧基与碳酸钠反应,E中亚甲基与甲醛发生加成反应、消去反应引入碳碳双键,最终生成F。
.对比E、F的结构,可知E的羧基与碳酸钠反应,E中亚甲基与甲醛发生加成反应、消去反应引入碳碳双键,最终生成F。
(6)模仿C→F的转化,可知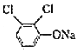 先与ClCH2COOH反应,产物再与CH3CH2CH2COCl/AlCl3、CS2作用,最后与HCHO反应得到目标物。
先与ClCH2COOH反应,产物再与CH3CH2CH2COCl/AlCl3、CS2作用,最后与HCHO反应得到目标物。
(1)![]() 中Cl为取代基,丙酸为母体从羧基中C原子起编碳号,名称为:2-氯丙酸;
中Cl为取代基,丙酸为母体从羧基中C原子起编碳号,名称为:2-氯丙酸;
(2)D为 ,D中含氧官能团的名称为:羧基、醚键;
,D中含氧官能团的名称为:羧基、醚键;
(3)B→C的反应方程式为: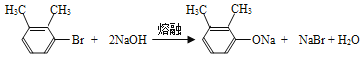
(4)D→E是苯环上H原子被-COCH2CH3替代,属于取代反应;
(5)C( )的同分异构体有多种,其中苯环上连有—ONa、2个—CH3的同分异构体,2个甲基有邻、间、对3种位置结构,对应的-ONa分别有2种、3种、1种位置结构,共有6种,不包括C本身还有5种,核磁共振氢谱为3组峰,峰面积之比为6:2:1的同分异构体的结构简式为:
)的同分异构体有多种,其中苯环上连有—ONa、2个—CH3的同分异构体,2个甲基有邻、间、对3种位置结构,对应的-ONa分别有2种、3种、1种位置结构,共有6种,不包括C本身还有5种,核磁共振氢谱为3组峰,峰面积之比为6:2:1的同分异构体的结构简式为: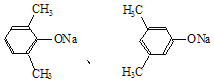 ;
;
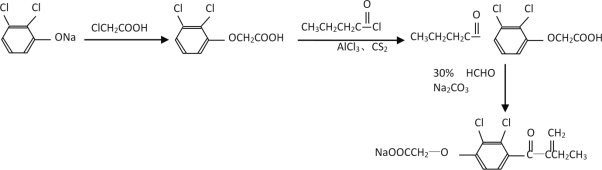
(6)模仿C→F的转化,可知 先与ClCH2COOH反应,产物再与CH3CH2CH2COCl/AlCl3、CS2作用,最后与HCHO反应得到目标物,合成路线流程图为:
先与ClCH2COOH反应,产物再与CH3CH2CH2COCl/AlCl3、CS2作用,最后与HCHO反应得到目标物,合成路线流程图为: 。
。


科目:高中化学 来源: 题型:
【题目】Na2S可用于制造硫化染料、沉淀水体中的重金属等。
(1)Na2S溶液中S2-水解的离子方程式为_________。
(2)室温时,几种重金属离子的硫化物的溶度积常数如下表:
金属硫化物 | FeS | PbS | CuS | HgS |
Ksp | 6.3×10-18 | 1.0×10-28 | 6.3×10-36 | 1.6×10-52 |
①向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是____。
②用Na2S溶液沉淀废水中Pb2+,为使Pb2+沉淀完全[c(Pb2+)≤1×10-6mol/L],则应满足溶液中c(S2-)≥_____mol/L。
③反应Cu2+(aq)+FeS(s)![]() Fe2+(aq)+CuS(s)的平衡常数K=_______。
Fe2+(aq)+CuS(s)的平衡常数K=_______。
(3)测定某Na2S和NaHS混合样品中两者含量的实验步骤如下:
步骤1.准确称取一定量样品于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容。
步骤2.准确移取25.00mL上述溶液于锥形瓶中,加入茜素黄GG-百时香酚蓝混合指示剂,用0.2500mol/L盐酸标准溶液滴定(Na2S+HCl=NaHS+NaCl)至终点,消耗盐酸24.00mL;向其中再加入5mL中性甲醛(NaHS+HCHO+H2O→NaOH+HSCH2OH)和3滴酚酞指示剂,继续用0.2500mol/L盐酸标准溶液滴定(NaOH+HCl=NaCl+H2O)至终点,又消耗盐酸34.00mL。
计算原混合物中Na2S与NaHS的物质的量之比(写出计算过程)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从工业废钒中回收金属钒既避免污染环境又有利于资源综合利用。某工业废钒的主要成分为V2O5、VOSO4和SiO2等,下图是从废钒中回收钒的一种工艺流程:

(1)为了提高“酸浸”效率,可以采取的措施有________(填两种).
(2)“还原”工序中反应的离子方程式为________.
(3)“沉钒”得到NH4VO3沉淀,需对沉淀进行洗涤,检验沉淀完全洗净的方法是________.
(4)写出流程中铝热反应的化学方程式________.
(5)电解精炼时,以熔融NaCl、CaCl2和VCl2为电解液(其中VCl2以分子形式存在).粗钒应与电源的________极(填“正”或“负”)相连,阴极的电极反应式为________.
(6)为预估“还原”工序加入H2C2O4的量,需测定“酸浸”液中VO2+的浓度.每次取25.00mL“酸浸”液于锥形瓶用a mol/L(NH4)2Fe(SO4)2标准溶液和苯代邻氨基苯甲酸为指示剂进行滴定(其中VO2+ VO2+),若三次滴定消耗标准液的体积平均为bmL,则VO2+的浓度为________g/L(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用资源,降低碳的排放,实施低碳经济是今后经济生活主流方向。
(1)下列措施不利于有效减少二氧化碳排放的是________。
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用石油液化气
C.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
D.倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率
(2)CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。进行如下实验:某温度下在1 L的密闭容器中,充2 mol CO2和6 mol H2,发生:CO2(g)+3H2(g )![]() CH3OH(g)+H2O(g),现测得CO2和CH3OH(g)的浓度随时间变化如下图1所示。从反应开始到平衡时CO2的转化率为_________。氢气的平均反应速率v(H2)=_______mol/(L·min)。该温度下的平衡常数为________。
CH3OH(g)+H2O(g),现测得CO2和CH3OH(g)的浓度随时间变化如下图1所示。从反应开始到平衡时CO2的转化率为_________。氢气的平均反应速率v(H2)=_______mol/(L·min)。该温度下的平衡常数为________。
(3)CO在催化作用下生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如图所示。
CH3OH(g)。已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如图所示。
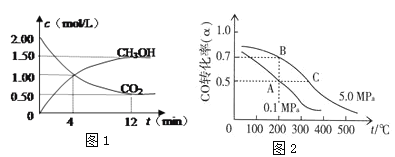
①该反应的ΔH_____0;ΔS____0。 (填“>、=、<”)
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA ____ tC(填“>、=、<”)
③A、B、C三点对应的平衡常数分别为KA、KB、KC,则的大小关系是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图2),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。

Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为_________,B→C的反应条件为__________,C→Al的制备方法称为______________。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)___________。
a.温度 b.Cl-的浓度 c.溶液的酸度
(3)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
Ⅱ.含铬元素溶液的分离和利用
(4)用惰性电极电解时,CrO42-能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;阴极室生成的物质为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷燃料电池体积小巧、燃料使用便利、洁净环保、理论能量比高,用甲烷燃料电池为下图电解装置供电,工作一段时间后,A池中左右试管收集到的气体体积比为2:1,则:
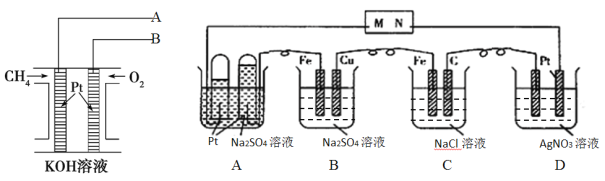
(1)电解一段时间后,甲烷燃料电池中溶液的pH_________。(填“增大、减小或不变”)
(2)甲烷燃料电池中导线A与电解池中的_________(填M或N)导线连接
(3)B池中一段时间后实验现象______________________________________________。
(4)相同条件下,电解质足量的A、B、C、D池中生成气体的总体积由大到小的顺序为_______。
(5)D池电解一段时间后,若要使电解质溶液恢复到电解前的状态,可加入________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
铜矿( CuFeS2)是炼铜的最主要矿物。火法冶炼黄钢矿的过程中,其中一步反应是:2Cu2O+Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+价电子的电子排布图为___________,Cu2O与Cu2S比较,熔点较高的是___________,原因为______________________。
(2)SO2与SO3的键角相比,键角更小的是___________。某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图1所示。此固态物质中S原子的杂化轨道类型是___________;该物质的化学式为___________。

(3)离子化合物CaC2的晶体结构如图2所示。写出该物质的电子式___________。从钙离子看该晶体属于___________堆积,一个晶胞含有的π键平均有___________个。

(4)根据图3可知,与每个C60分子距离最近且相等的C60分子有___________个,其距离为___________cm(列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
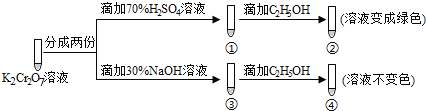
结合实验,下列说法错误的是( )
A.①中溶液橙色加深,③中溶液变黄B.对比②和④可知K2Cr2O7酸性溶液氧化性强
C.②中C2H5OH使Cr2O72-被氧化D.若向④中加入70%H2SO4溶液至过量,溶液可变为绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:
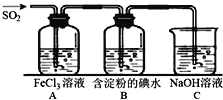
(1)写出由铜和浓硫酸制取SO2的化学方程式_____________________。
(2)装置A中的现象是__________。若要从A中的FeCl3溶液中提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在过滤操作中有用到的玻璃仪器有_______(填编号)。
A酒精灯 B烧瓶 C漏斗 D烧杯 E玻璃棒 F坩埚
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式___________________;
②请设计实验方案检验有Fe2+生成__________________________;
(4)B中蓝色溶液褪色,表明I-的还原性比SO2__________(填“强”或“弱”)。
(5)若C中所得溶液只有一种溶质且pH>7,则溶液中各离子浓度大小顺序为_________。
(6)工业上通过煅烧黄铁矿产生SO2来进一步得到硫酸,已知煅烧1g FeS2产生7.1kJ热量,写出煅烧FeS2的热化学反应方程式____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com