
分析 n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol,与硝酸反应生成Cu(NO3)2、NO和NO2,气体的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,结合N元素守恒、电子守恒计算.
解答 解:n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol,气体的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,
(1)由N原子守恒可知,原子守恒得生成硝酸铜需要的n(HNO3)=2n[Cu(NO3)2]=2n(Cu)=2×0.3mol=0.6mol,气体为氮氧化物,气体的物质的量=n(NO)+n(NO2)=0.5mol,根据N元素守恒可知共消耗硝酸的物质的量为0.6mol+0.5mol=1.1mol,
答:消耗HNO3的物质的量为1.1mol;
(2)设NO2和NO各为x、y,
由原子守恒及电子守恒可知,
$\left\{\begin{array}{l}{x+y=0.5}\\{x+3y=0.3×2}\end{array}\right.$,
解得x=0.45mol,y=0.05mol,
答:11.2升气体中NO2和NO各为0.45mol、0.05mol.
点评 本题考查氧化还原反应的计算,为高频考点,把握电子守恒、原子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:选择题
| A. | 活化能的大小对化学反应前后的能量变化不产生影响 | |
| B. | 化学键的断裂和形成是物质在化学变化中发生能量变化的主要原因 | |
| C. | 盐酸和NaOH(aq)反应的中和热△H=-57.3kJ/mol,则H2SO4(aq)和Ca(OH)2(aq)反应的中和热△H=2×(-57.3)kJ/mol | |
| D. | CO(g)的燃烧热是283.0kJ/mol,则反应2CO2(g)=2CO(g)+O2(g)的反应热△H=+2 x283.0kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaCl(aq)+AgNO3(aq)=AgCl(s)+NaNO3(aq )△H<0 | |
| B. | 2KMnO4(s)=2K2MnO4(s)+MnO2(s)+O2(g)△H>0 | |
| C. | 2FeCl3(aq)+Fe(s)=3FeCl3(aq)△H<0 | |
| D. | 2H2(g)+O2(g)=2H2O (l)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
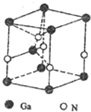 碳、氮元素及其化合物在生产、生活和科学研究等方面有着重要的作用研究它们的结构与性质意义重大.请回答下列有关问题:
碳、氮元素及其化合物在生产、生活和科学研究等方面有着重要的作用研究它们的结构与性质意义重大.请回答下列有关问题: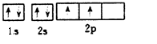 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H1 | B. | S(s)+3/2O2(g)=SO3(s)△H2 | ||
| C. | CH4(g)+2O2(g)=2H2O(l)+CO(g)△H3 | D. | 2CO(g)+O2(g)=CO2(g)△H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
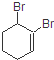 的系统命名的名称是( )
的系统命名的名称是( )| A. | 1,2-二溴-2-环己烯 | B. | 1,2-二溴-1-环己烯 | ||
| C. | 1,6-二溴-1-环己烯 | D. | 2,3-二溴-1-环己烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵与苯分别受热变为气体 | B. | 氯化钠与氯化氢分别溶解在水中 | ||
| C. | 碘与干冰分别受热变为气体 | D. | NaHSO4受热熔化与溶于水变为溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com