
【题目】在一定温度下,向5L密闭容器中加入2mol Fe(s)与1mol H2O(g),t1秒时,H2的物质的量为0.20mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35mol.
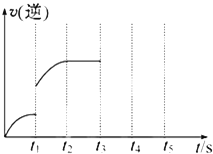
(1)t1~t2这段时间内的化学反应速率v(H2)=________
(2)保持温度不变,若继续加入2mol Fe(s),则平衡移动________ (填“向正反应方向”、“向逆反应方向”或“不”),继续通入1mol H2O(g)再次达到平衡后,H2物质的量为________ mol.
(3)该反应在t3时刻改变了某种条件使逆反应速率增大,改变的条件可能是________(任填一个即可)
(4)该反应的平衡常数表达式________
【答案】0.03/(t2-t1)molL﹣1s﹣1 不 0.7 升高温度 ![]()
【解析】
铁与水蒸气反应的方程式为3Fe(s)+4H2O(g)Fe3O4 (s)+4H2 (g),该反应前后气体分子数不发生变化,故在一定的范围内改变压强不会使平衡发生移动。该反应的平衡常数表达式为:K![]() 。
。
(1)t1 ~t2 这段时间内氢气的浓度变化为:0.35mol-0.20mol=0.15mol,这段时间内的化学反应速率v(H2)=0.15/[5×(t2- t1)]= 0.03/(t2-t1)molL﹣1s﹣1;综上所述,本题答案是:0.03/(t2-t1)molL﹣1s﹣1。
(2)在固体有剩余的情况下,增加或减少固体的质量,对反应速率以及限度均无影响;再加入1molH2O(g) 再次达到平衡时,平衡常数不变,故H2 的物质的量为原来的2倍,即:H2 物质的量为0.35×2=0.7mol;综上所述,本题答案是:不;0.7。
(3)t1 时反应未达到平衡,改变条件后逆反应速率突然增大,且继续增大,改变的条件为升高温度;综上所述,本题答案是:升高温度。
(4)铁与水蒸气反应的方程式为:3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g),平衡常数表达式为:K![]() ;综上所述,本题答案是: K
;综上所述,本题答案是: K![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列化学反应中,同时存在离子键、极性键、非极性键的断裂与生成的是
A.2Na2O2+2H2O=4NaOH+O2↑B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
C.Cl2+H2O=HClO+HClD.NH4Cl+NaOH=NaCl+NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定条件下,合成氨反应为:N2(g)十3H2(g)![]() 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时 间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.下列说法正确的是
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时 间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.下列说法正确的是
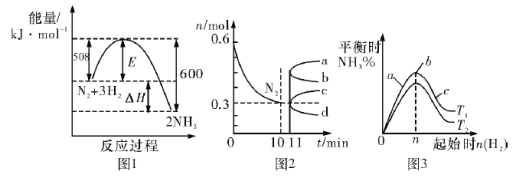
A.升高温度,该反应的平衡常数增大
B.由图2信息,10 min内该反应的平均速率![]() (H2)=0.09 mol L-1 min-1
(H2)=0.09 mol L-1 min-1
C.由图2信息,从11 min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为d
D.图3中温度T1<T2,a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素类化合物M具有抗病毒、抗癌等多种生物活性。下图是M和聚合物E的合成路线。
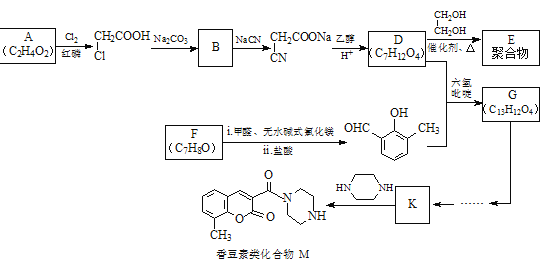
已知:
① ![]()
② ![]()
③ 
(1)A中官能团是_______。
(2)B→![]() 的反应类型是________。
的反应类型是________。
(3)化合物F能与FeCl3溶液发生显色反应,其结构简式是________。F有多种同分异构体,其中属于芳香族化合物、且为醇类物质的结构简式是________。
(4)G的结构简式是________。
(5)D→聚合物E的化学方程式是________。
(6)已知![]() ,将下列G→K的流程图补充完整:_____________________
,将下列G→K的流程图补充完整:_____________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两种气体的原子数一定相等的是
A. 质量相等、密度不等的N2和C2H4
B. 等体积、等密度的CO和N2
C. 等温、等体积的O2和Cl2
D. 等压、等体积的NH3和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表的说法正确的是( )
A.周期表的每一个纵列代表一个独立的族
B.主族元素中没有都是金属元素的族
C.副族元素都是金属元素
D.周期表共有14个族
查看答案和解析>>
科目:高中化学 来源: 题型:
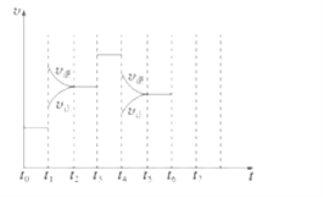
【题目】在一密闭容器中发生反应N2+3H22NH3 ,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
(1)处于平衡状态的时间段是________(填选项).
A.t0~t1 B.t1~t2 C.t2~t3 D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.充入氮气
t1时刻________;t3时刻________;t4时刻________.
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是________(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,此时正向速率________逆向速率(填大于、小于、等于),平衡________移动(填正向、逆向、不移动)。
(5)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1L密闭容器中有0.1molSO2和0.05molO2发生反应,恒温下30min后达到平衡。
(1)若得到0.06molSO3,求达到平衡时SO2的浓度_______。
(2)求30min内的反应速率:v(SO3)、v(O2)_______。
(3)求平衡时气体压强与开始时气体压强之比_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫元素的几种化合物存在下列转化关系:
![]()
下列判断不正确的是
A. 反应①中浓硫酸作氧化剂 B. 反应②表明SO2有酸性氧化物的性质
C. 反应③的原子利用率是100% D. 反应④稀H2SO4作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com