
【题目】下列反应的离子方程式书写正确的是( )
A. 向氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=4AlO2-+4NH4++2H2O
B. 用硫化亚铁与稀硫酸反应制硫化氢:S2-+2H+=H2S↑
C. 双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
D. 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
【答案】C
【解析】本题是对离子反应方程式书写正误判断的考查,离子反应及其方程式的书写是高考的必考内容,要求学生掌握其书写方法,注意事项,与量有关的反应注意产物的类型等。
A.氢氧化铝与氨水不能反应,应为:Al3++3NH3·H2O=Al(OH)3↓+3NH4+,故A错误;
B. 硫化亚铁是难溶于水的物质不能拆成离子,应为:FeS+2H+=Fe2++H2S↑;故B错误;
C. 双氧水加入稀硫酸和KI溶液,由于双氧水具有氧化性,负一价碘离子具有还原性,会发生氧化还原反应:H2O2+2H++2I-=I2+2H2O,所以C正确;
D. 向NH4HCO3溶液中加入过量的NaOH溶液并加热,碳酸氢铵溶液中的铵根离子和碳酸氢根离子均能与氢氧化钠反应,其反应的离子方程式为:NH4++HCO3-+2OH-![]() CO32-+2H2O+NH3↑,所以D错误。
CO32-+2H2O+NH3↑,所以D错误。
故答案为:C。


科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2 , 其工作原理如图所示.下列说法正确的是( ) 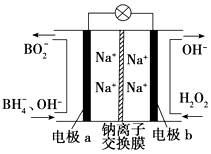
A.每消耗1 mol H2O2 , 转移的电子为1 mol
B.电极b采用MnO2 , MnO2既作电极材料又有催化作用
C.该电池的正极反应为BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2O
D.电池放电时Na+从b极区移向a极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,不正确的是( )
A. 实验室用过氧化氢分解制氧气,加入二氧化锰,反应速率明显加快
B. 在金属钠与足量水反应中,增加水的量能加快反应速率
C. 2SO2+O2![]() 2SO3反应中,增加二氧化硫的量可加快反应速率
2SO3反应中,增加二氧化硫的量可加快反应速率
D. 实验室用碳酸钙和盐酸反应制取二氧化碳,用碳酸钙粉末比块状反应要快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,有关叙述不正确的是( )
① | ② | ③ | ④ | |
浓度c/mol/L | 0.1 | 0.1 | 0.1 | 0.1 |
溶液 | 氨水 | CH3COONa溶液 | 醋酸 | 盐酸 |
A.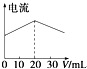 在20 mL ①溶液中逐滴加入③溶液,溶液导电能力变化如图
在20 mL ①溶液中逐滴加入③溶液,溶液导电能力变化如图
B.②、③两溶液等体积混合,离子浓度:2c(Na+)=c(CH3COO﹣)+c(CH3COOH)
C.①、④两溶液等体积混合,离子浓度:c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
D.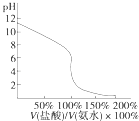 用④滴定①,滴定曲线如图,可用酚酞作指示剂
用④滴定①,滴定曲线如图,可用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.1molO的质量是16g/molB.Na+的摩尔质量是23g/mol
C.CO2的摩尔质量是44D.H2的摩尔质量就是相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】性激素是一种固醇类物质,它可以优先通过细胞膜扩散到细胞内部,这主要与细胞的哪项结构或功能有关
A. 膜表面的糖蛋白 B. 膜内含有相应的载体多
C. 膜的选择透过性 D. 膜的基本骨架为脂双层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2、CO、CH4、CH3OH等都是重要的能源,也是重要为化工原料。
(1)已知25℃,1.01×105Pa时,,8.0DgCH4完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写山该反应的热化学反应方程式:____________________。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。
在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
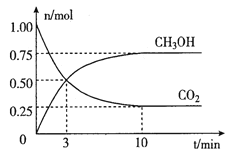
①从反或开始到平衡,CO2的平均反应速率v(CO2)=____。
②达到平衡时,H2的转化率为__________。
③下列措施不能提高反应速率的是__________。
A.升高温度 B.加入催化剂 C.增大压强 D.及时分离出CH3OH
(3)工业上也用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)![]() CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1mclCH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com