
| A. | v(NH3)=0.2 mol•L-1•s-1 | B. | v(N2)=1.0 mol•L-1•min-1 | ||
| C. | v(H2)=1.67 mol•L-1•min-1 | D. | v(H2)=0.3 mol•L-1•min-1 |
分析 该时间内v(NH3)=$\frac{0.6-0}{3}$mol•L-1•min-1=0.2 mol•L-1•min-1,再根据同一可逆反应同一时间段内各物质的反应速率之比等于其计量数之比计算氢气、氮气反应速率,据此分析解答.
解答 解:该时间内v(NH3)=$\frac{0.6-0}{3}$ mol•L-1•min-1=0.2 mol•L-1•min-1,再根据同一可逆反应同一时间段内各物质的反应速率之比得v(N2)=$\frac{1}{2}$×v(NH3)=$\frac{1}{2}$×$\frac{0.6-0}{3}$ mol•L-1•min-1=0.1 mol•L-1•min-1,
v(H2)=$\frac{3}{2}$×0.2 mol•L-1•min-1=$\frac{3}{2}$×$\frac{0.6-0}{3}$ mol•L-1•min-1=0.3mol•L-1•min-1,
A.v(NH3)=0.2 mol•L-1•min-1=0.0033mol•L-1•s-1,故A错误;
B.v(N2)=$\frac{1}{2}$×v(NH3)=$\frac{1}{2}$×$\frac{0.6-0}{3}$ mol•L-1•min-1=0.1 mol•L-1•min-1,故B错误;
C.v(H2)=$\frac{3}{2}$×0.2 mol•L-1•min-1=$\frac{3}{2}$×$\frac{0.6-0}{3}$ mol•L-1•min-1=0.3mol•L-1•min-1,故C错误;
D.v(H2)=$\frac{3}{2}$×0.2 mol•L-1•min-1=$\frac{3}{2}$×$\frac{0.6-0}{3}$ mol•L-1•min-1=0.3mol•L-1•min-1,故D正确;
故选D.
点评 本题考查化学反应速率计算,侧重考查分析计算能力,明确各物质反应速率与计量数关系即可解答,注意单位换算,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
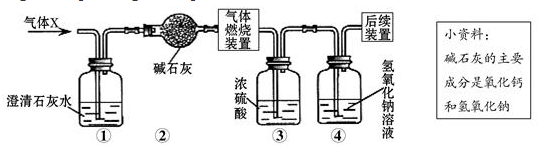
| A. | 一定没有二氧化碳 | B. | 可能含有甲烷和氢气 | ||
| C. | 可能只有甲烷 | D. | 可能含有氢气和一氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑧ | B. | ④⑤⑦ | C. | ④⑤⑧ | D. | ③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
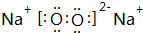 ,该氧化物与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑.
,该氧化物与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
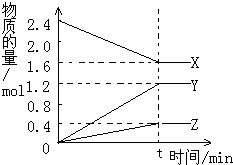 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是吸热反应 | B. | 是放热反应 | ||
| C. | 是熵减小的反应 | D. | 熵增效应大于热效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com