
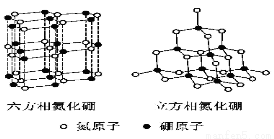
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。
⑴基态硼原子的电子排布式为 。
⑵ 关于这两种晶体的说法,正确的是 (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大 b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键 d.两种晶体均为分子晶体
⑶六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为 ,其结构与石墨相似却不导电,原因是 。
⑷立方相氮化硼晶体中,硼原子的杂化轨道类型为 。该晶体的天然矿物在青藏高原在下约300Km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
⑸NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有 mol配位键。
⑴1s22s22p1
⑵b、c
⑶平面三角形 层状结构中没有自由移动的电子
⑷sp3 高温、高压
⑸2
【解析】
试题分析:
⑴硼的原子序数为5,故其基态硼原子的电子排布式为1s22s22p1。
⑵a项立方相氮化硼只含有σ键,错误;b项六方相氮化硼层间存在分子间作用力,该作用力小(同石墨),质地软,正确;c项两种晶体中的B-N键均为共价键,正确;d项立方相氮化硼属于原子晶体,错误。
⑶六方相氮化硼晶体层内一个硼原子与相邻3个氮原子形成3个σ键,无孤对电子,其构成的空间构型为平面三角形;其结构与石墨相似,但六方相氮化硼晶体的层状结构中没有自动移动的电子,故不导电。
⑷立方相氮化硼晶体中,硼原子与相邻4个氮原子形成4个σ键(其中有1个配位键),故硼原子的杂化轨道类型为sp3;根据“含立方相氮化硼晶体的天然矿物在青藏高原在下约300Km的古地壳(在高温、高压环境下)中被发现”,可推断实验室由六方相氮化硼合成立方相氮化硼需要的条件是“高温、高压”。
⑸NH4BF4(氟硼酸铵)含有NH4+ 、BF4- 离子,1个NH4+ 离子中含有1个配位键,1个BF4- 离子中也含有1个配位键,故1mo NH4BF4含有2 mol配位键。
考点:考查物质结构与性质(基态原子的电子排布式、晶体类型、微粒的空间构型、中心原子的杂化方式、配位键)。


科目:高中化学 来源:2013-2014北京市第二学期期中测试高二化学试卷(解析版) 题型:选择题
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是
A.CH3CH2CH3 B.CH3CH2COCH2CH3
C.CH3OCH3 D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市第二学期期中测试高二化学试卷(解析版) 题型:选择题
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如下图,下列对该化合物叙述正确的是
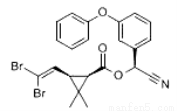
A.属于芳香烃 B.属于卤代烃
C.属于高分子化合物 D.属于有机化合物
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(重庆卷解析版) 题型:选择题
茶叶中铁元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是
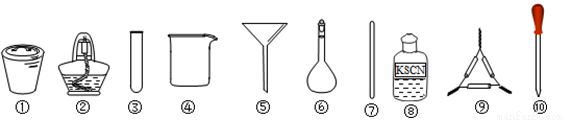
A.将茶叶灼烧灰化,选用①、②和⑨
B.用浓硝酸溶解茶叶并加蒸馏水稀释,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验中滤液中的Fe3+,选用③、⑧和⑩
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(福建卷解析版) 题型:选择题
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
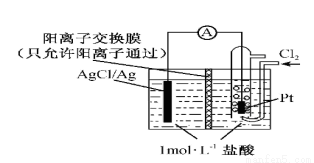
A.正极反应为AgCl +e-=Ag +Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(海南卷解析版) 题型:填空题
【选修3-物质结构与性质】(20分)
19-I(6分)对于钠的卤化物(NaX)和硅的卤化物(SiX4),下列叙述正确的是
A.SiX4难水解 B.SiX4是共价化合物
C.NaX易水解 D.NaX的熔点一般高于SiX4
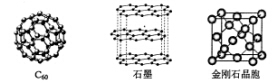
19-Ⅱ(14分)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
回答下列问题:
(1)金刚石、石墨、C60.碳纳米管等都是碳元素的单质形式,它们互为_____________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为____、____。
(3)C60属于____晶体,石墨属于____晶体。
(4)石墨晶体中,层内C-C键的键长为142 pm,而金刚石中C-C键的键长为154 pm。其原因是金刚石中只存在C-C间的____共价键,而石墨层内的C-C间不仅存在____共价键,还有____键。
(5)金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______a,列式表示碳原子在晶胞中的空间占有率____(不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(海南卷解析版) 题型:选择题
下列有关物质性质的说法错误的是
A.热稳定性:HCl> HI B.原子半径:Na> Mg
C.酸性:H2SO3>H2SO4。 D.结合质子能力:S2-> Cl-
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(新课标Ⅱ卷解析版) 题型:选择题
室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) △CuSO4(s)+5H2O(l), 热效应为△H3。则下列判断正确的是
A.△H2>△H3 B.△H1<△H3
C.△H1+△H3 =△H2 D.△H1+△H2 >△H3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com