
| A£® | SiH4±ČCH4ĪČ¶Ø | |
| B£® | O2- °ė¾¶±ČF- µÄŠ” | |
| C£® | NaŗĶCsŹōÓŚµŚ¢ńA×åŌŖĖŲ£¬CsŹ§µē×ÓÄÜĮ¦±ČNaµÄĒæ | |
| D£® | PŗĶSŹōÓŚµŚČżÖÜĘŚµÄŌŖĖŲ£¬H3PO4ĖįŠŌ±ČH2SO4µÄČõ |
·ÖĪö A£®Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀ£¬·Ē½šŹōŠŌ¼õČõ£¬·Ē½šŹōŠŌŌ½Čõ£¬¶ŌÓ¦µÄĒā»ÆĪļµÄĪČ¶ØŠŌŌ½Š”£»
B£®ŗĖĶāµē×ÓÅŲ¼ĻąĶ¬Ź±£¬Ō×ÓŠņŹżŌ½Š”£¬°ė¾¶Ō½“ó£»
C£®¼ī½šŹō“ÓÉĻµ½ĻĀ£¬ŌŖĖŲµÄ½šŹōŠŌÖš½„ŌöĒ棬Ź§Č„µē×ÓÄÜĮ¦ŌöĒ棻
D£®·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌŌ½Ē森
½ā“š ½ā£ŗA£®Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀ£¬·Ē½šŹōŠŌ¼õČõ£¬·Ē½šŹōŠŌC£¾Si£¬·Ē½šŹōŠŌŌ½Čõ£¬¶ŌÓ¦µÄĒā»ÆĪļµÄĪČ¶ØŠŌŌ½Š”£¬ĪČ¶ØŠŌ£ŗCH4£¾SiH4£¬¹ŹA“ķĪó£»
B£®ŗĖĶāµē×ÓÅŲ¼ĻąĶ¬Ź±£¬Ō×ÓŠņŹżŌ½Š”£¬°ė¾¶Ō½“ó£¬ĖłŅŌO2-°ė¾¶±ČF-µÄ“󣬹ŹB“ķĪó£»
C£®CsŹĒµŚ¢ńA×åŌŖĖŲ£¬ĪŖ¼ī½šŹō£¬CsŹ§µē×ÓÄÜĮ¦±ČNaµÄĒ棬¹ŹCÕżČ·£»
D£®·Ē½šŹōŠŌS£¾P£¬·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌŌ½Ē棬ĖįŠŌ£ŗH2SO4£¾H3PO4£¬¹ŹDÕżČ·£®
¹ŹŃ”CD£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲŠŌÖŹµÄ±Č½Ļ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄ½šŹōŠŌ”¢·Ē½šŹōŠŌ±Č½ĻĪŖ½ā“šµÄ¹Ų¼ü£¬×¢ŅāŌŖĖŲµÄĪ»ÖĆ¼°ŌŖĖŲÖÜĘŚĀɵÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹÆøąÄÜŹ¹¶¹½¬±ä³É¶¹øÆ | |
| B£® | Ć÷·Æ¾»Ė® | |
| C£® | »Ø·ŪŌŚĖ®ĆęÉĻ×ö²¼ĄŹŌĖ¶Æ | |
| D£® | Ģ«Ńō¹āÕÕŌŚĆÖĀž»Ņ³¾µÄŹŅÄŚ£¬æÉ擵½“Ó“°æŚµ½µŲĆę³öĻÖŅ»Ģõ¹āĮĮµÄĶØĀ· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ¬1molNa2SµÄČÜŅŗ£¬×ī¶ąæÉĪüŹÕ2molSO2 | |
| B£® | æÉŅŌÓĆÅØĮņĖį³żČ„¶ĘŌŚĀĮ±ķĆęµÄĶ¶Ę²ć | |
| C£® | Li”¢C”¢S·Ö±šŌŚ×ćĮæŃõĘųÖŠČ¼ÉÕ¾łÉś³ÉŅ»ÖÖĻąÓ¦Ńõ»ÆĪļ | |
| D£® | NaHCO3”¢Na2CO3”¢£ØNH4£©2CO3ČżÖÖ¹ĢĢåŹÜČČŗó¾łÄÜÉś³ÉĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪĀ¶Č | B£® | ÅØ¶Č | C£® | “߻ƼĮ | D£® | ·“Ó¦ĪļµÄŠŌÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ŃĪĒÅÖŠµÄK+ŅĘĻņZnSO4ČÜŅŗ | |
| B£® | 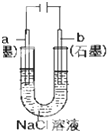 ¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬a¼«ø½½üČÜŅŗµÄC£ØOH-£©Ōö“ó | |
| C£® | 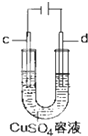 ¹¤×÷Ź±£¬c¼«ĪŖ·¢ÉśŃõ»Æ·“Ó¦ | |
| D£® |  µē×ÓÓÉZnĮ÷ĻņFe£¬×°ÖĆÖŠÓŠFe2+Éś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĻÖÓŠA”¢BĮ½ÖÖ½šŹō·Ö±šÓėŃĪĖį·“Ó¦£¬²śÉśĒāĘųµÄĖŁĀŹĻą½ü£®ĒėÉč¼ĘŅ»øöŌµē³ŲŹµŃéÖ¤Ć÷A”¢BĮ½ÖÖ½šŹōµÄ»ī¶ÆŠŌ£æ£Øµē¼«²ÄĮĻ£ŗA”¢B£¬µē½āÖŹČÜŅŗ£ŗŃĪĖį£¬ĘäĖüŹµŃéÓĆĘ·æÉ×ŌŃ”£©£¬ĒėŌŚ·½æņÖŠ»³ö¼ņŅ××°ÖĆĶ¼£®ČēAŹĒ½Ļ²»»īĘĆµÄ½šŹō£¬ŌņAµÄĻÖĻóŹĒÓŠĘųÅŻŅŻ³ö£¬ÄĒĆ“£¬B¼“ŹĒ»īĘĆµÄ½šŹō£®
ĻÖÓŠA”¢BĮ½ÖÖ½šŹō·Ö±šÓėŃĪĖį·“Ó¦£¬²śÉśĒāĘųµÄĖŁĀŹĻą½ü£®ĒėÉč¼ĘŅ»øöŌµē³ŲŹµŃéÖ¤Ć÷A”¢BĮ½ÖÖ½šŹōµÄ»ī¶ÆŠŌ£æ£Øµē¼«²ÄĮĻ£ŗA”¢B£¬µē½āÖŹČÜŅŗ£ŗŃĪĖį£¬ĘäĖüŹµŃéÓĆĘ·æÉ×ŌŃ”£©£¬ĒėŌŚ·½æņÖŠ»³ö¼ņŅ××°ÖĆĶ¼£®ČēAŹĒ½Ļ²»»īĘĆµÄ½šŹō£¬ŌņAµÄĻÖĻóŹĒÓŠĘųÅŻŅŻ³ö£¬ÄĒĆ“£¬B¼“ŹĒ»īĘĆµÄ½šŹō£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
 ŌŚČŻ»żŗć¶ØµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ·“Ó¦ 2NO+O2=2NO2 øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹĖꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®Čōt2”¢t4Ź±æĢÖ»øıäŅ»øöĢõ¼ž£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŌŚČŻ»żŗć¶ØµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ·“Ó¦ 2NO+O2=2NO2 øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹĖꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®Čōt2”¢t4Ź±æĢÖ»øıäŅ»øöĢõ¼ž£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌŚt5Ź±£¬ČŻĘ÷NO2µÄĢå»ż·ÖŹżŹĒÕūøö¹ż³ĢÖŠµÄ×ī“óÖµ | |
| B£® | ŌŚt2Ź±£¬²ÉČ”µÄ“ėŹ©æÉŅŌŹĒŌö“óŃ¹Ēæ | |
| C£® | ŌŚt3”«t4Ź±£¬æÉŅĄ¾ŻČŻĘ÷ÄŚĘųĢåµÄĆܶȱ£³Ö²»±äÅŠ¶Ļ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬ | |
| D£® | ŌŚt1”«t2Ź±£¬æÉŅĄ¾ŻČŻĘ÷ÄŚĘųĢåµÄŃ¹Ēæ±£³Ö²»±äÅŠ¶Ļ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ±ź×¼×“æöĻĀµ±¼×ÖŠ²śÉś4.48 LĘųĢåŹ±£¬±ūÖŠCuµē¼«ÖŹĮæŌö¼Ó21.6g | |
| B£® | µē½ā¹ż³ĢÖŠ±ūÖŠČÜŅŗpHĪŽ±ä»Æ | |
| C£® | Ļņ¼×ÖŠ¼ÓČėŹŹĮæµÄŃĪĖį£¬æÉŹ¹ČÜŅŗ»Öø“µ½µē½āĒ°µÄדĢ¬ | |
| D£® | ŅŅÖŠ×ó²ąµē¼«·“Ó¦Ź½£ŗCu2++2e-ØTCu |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļņ±„ŗĶĀČĖ®ÖŠĶØČėHCl£¬ÓŠc£ØH+£©ØTc£ØCl-£©+c£ØOH-£©+c£ØClO-£© | |
| B£® | ĀČĘųŌŚ1mol•L-1µÄNaClČÜŅŗÖŠ±ČŌŚ1mol•L-1µÄAlCl3ČÜŅŗÖŠµÄČܽā¶ČŠ” | |
| C£® | ¹āÕÕ£¬ĀČĖ®µÄĘư׊ŌŌöĒæ | |
| D£® | ČōĻņ±„ŗĶĀČĖ®ÖŠĶØČėÉŁĮæH2S£¬Ōņ$\frac{c£Ø{H}^{+}£©}{c£ØClO^-£©}$¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com