
可逆反应: (正反应是吸热反应),随着温度升高,气体平均相对分子质量有减小趋势,则下列判断正确的是
(正反应是吸热反应),随着温度升高,气体平均相对分子质量有减小趋势,则下列判断正确的是
[ ]
A.B和C可能都是固体
B.B和C一定都是气体
C.若C为固体,则B一定是气体
D.B和C可能都是气体
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
A.加催化剂,v(正)、v(逆)都发生变化,且变化的倍数相等
B.加压,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
C.降温,v(正)、v(逆)减小,且v(正)减小的倍数大于v(逆)减小的倍数
D.体积不变,加入氩气,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,可逆反应N2+3H2![]() 2NH3(正反应是放热反应)达到平衡,当单独改变下列条件后,有关叙述错误的是( )
2NH3(正反应是放热反应)达到平衡,当单独改变下列条件后,有关叙述错误的是( )
A.加催化剂,v(正)、v(逆)都发生变化,且变化的倍数相等
B.加压,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
C.降温,v(正)、v(逆)减小,且v(正)减小的倍数大于v(逆)减小的倍数
D.体积不变,加入氩气,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
查看答案和解析>>
科目:高中化学 来源:2011-2012年广东省汕头市高二上学期期中考试化学试卷(理科) 题型:选择题
下列可逆反应中,正反应是吸热反应的是
A.PCl3(l)+Cl2(g) PCl5(s) 降温,PCl3转化率增大
PCl5(s) 降温,PCl3转化率增大
B.NO2(g)+SO2(g) NO(g)+SO3(g) 降温,SO3的体积分数增加
NO(g)+SO3(g) 降温,SO3的体积分数增加
C.2NO2 (g) 2NO(g)+O2(g) 降温,颜色加深
2NO(g)+O2(g) 降温,颜色加深
D.CS2(l)+2H2O(g) CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
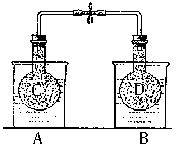 NO2和N2O4的混合气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把烧瓶C放人A烧杯中,烧瓶D放人B烧杯中。
NO2和N2O4的混合气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把烧瓶C放人A烧杯中,烧瓶D放人B烧杯中。 N2O4(g)
N2O4(g)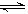 2NO2(g)达到化学平衡状态时压强变为1.515×105Pa,则平衡混合气体的平均相对分子质量为___________(精确到小数点后两位)。
2NO2(g)达到化学平衡状态时压强变为1.515×105Pa,则平衡混合气体的平均相对分子质量为___________(精确到小数点后两位)。查看答案和解析>>
科目:高中化学 来源: 题型:
下列可逆反应中,正反应是吸热反应的是
A.PCl3(l)+Cl2(g)PCl5(s) 降温,PCl3转化率增大
B.NO2(g)+SO2(g)NO(g)+SO3(g) 降温,SO3的体积分数增加
C.2NO2 (g)2NO(g)+O2(g) 降温,颜色加深
D.CS2(l)+2H2O(g)CO2(g)+2H2S(g) 升温,CO2的平衡浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com