
用物质的量都是0.1 mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中
c(CH3COO-)>c(Na+),对该混合溶液的下列判断正确的是
A. c(H+)>C(OH-)
B. c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
C. c(CH3COOH)>c(CH3COO-)
D. c(CH3COO-)+c(OH-)=0.2 mol·L-1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届陕西省高三上学期第二次模考化学试卷(解析版) 题型:选择题
Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e═Li2S+Fe ,有关该电池的下列中,正确的是
A. Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价
B. 该电池的电池反应式为:2Li + FeS = Li2S + Fe
C. 负极的电极反应式为Al-3e-=Al3+
D. 充电时,阴极发生的电极反应式为:Li2S + Fe -2e- = 2Li+ + FeS
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一下学期开学考试化学试卷(解析版) 题型:填空题
铁和铝是日常生活中用途广泛的金属。
I.(1)向NaAlO2溶液中滴加AlCl3溶液,生成白色胶状沉淀,则发生反应的离子方程式为_________________________。
(2)实验室常用还原性 Fe 粉与水蒸气反应的实验来研究 Fe 的还原性,则该反应的化学方程式为_________________________。
(3)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________________。
II.已知合金A由两种常见金属组成。为测定其组成,某同学的实验流程如图所示:
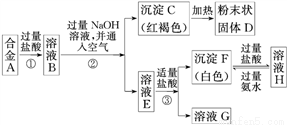
请回答:
(4)溶液E中所含的溶质是_________________(写化学式)
(5)合金A中的一种金属可以与粉末状固体D在高温下反应生成合金A中的另一种金属,请写出该反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列实验中,操作和现象均正确且能实现相应实验目的的是
选项 | 实验目的 | 操作 | 现象 |
A | 验证BaSO3难溶于水 | 将SO2通人Ba(NO3)2溶液中 | 有白色沉淀生成 |
B | 验证非金属性:Br>I | 将溴水滴加到淀粉KI溶液中 | 溶液变蓝 |
C | 验证SO2的漂白性 | 将SO2通入酸性KMnO4溶液中 | KMnO4溶液褪色 |
D | 验证某化合物一定是钠盐 | 将该化合物在酒精灯上灼烧 | 焰色为黄色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:填空题
已知25℃、101kPa时,一些物质的燃烧热为:
化学式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
ΔH/(kJ/mol) | -283.0 | -285.8 | -726.51 | -890. 31 |
请回答下列问题:
(1)根据盖斯定律完成下列反应的热化学方程式:
CO(g)+2H2(g)==CH3OH(l) ΔH=_________。
(2)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3 242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:____________。
A.1:1 B.1:3 C.1:4 D.2:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
用标准的NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是( )
A. 配制标准溶液的固体NaOH中混有杂质KOH
B. 盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
C. 滴定终点读数时,俯视滴定管的刻度,其他操作正确
D. 滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
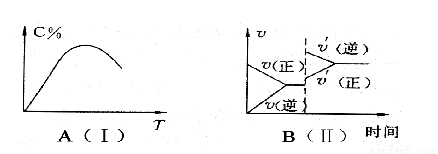
如图(Ⅰ)表示反应:mA(g)+nB(g)  pC(g)+qD(g);△H。在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系。图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变影响平衡的另一个条件,重新建立平衡的反应过程。由此可判断该反应中
pC(g)+qD(g);△H。在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系。图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变影响平衡的另一个条件,重新建立平衡的反应过程。由此可判断该反应中
A. m+n>p+q, 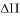 <0
<0
B. m+n>p+q, 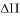 >0
>0
C. m+n<p+q, 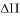 >0
>0
D. m+n<p+q, 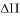 <0
<0
查看答案和解析>>
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:选择题
将一定量的氨基甲酸置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
A. 在低温下该反应能自发进行
B. 15℃时,该反应的化学平衡常数约为2.0
C. 当混合气体平均相对分子质量不变时,该反应达到化学反应限度
D. 恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变
查看答案和解析>>
科目:高中化学 来源:2017届河北省唐山市高三下学期第一次模拟考试理综化学试卷(解析版) 题型:推断题
【化学——选修5:有机化学基础】
某药厂在合成一种用于抑制血小板聚集的药物时使用到中间体有机物M,下图为有机物M(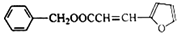 )的合成路线:
)的合成路线:
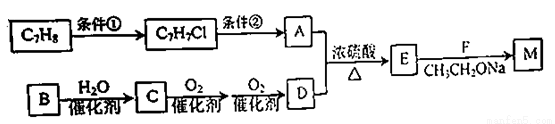
已知:①B是石油裂解的主要产物,其产量用于衡量化工发展的水平。
②R?—CHO+Rˊ—CH2COOR 
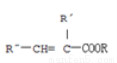
回答下列问题:
(1)E的化学名称是___________;C的官能团名称为____________。
(2)反应条件①为_____________。
(3)C7H7C1→A的化学方程式为____________________。
A+D→E的反应类型为________________。
(4)F分子的结构简式为________,其最多有______个原子共平面。
(5)能同时满足下列条件的M的同分异构体共有______种。(不含立体异构)
①属于苯的对位二取代衍生物,且与M具有相同官能团;②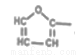 与苯环相连;③能够发生水解反应④能够发生银镜反应。
与苯环相连;③能够发生水解反应④能够发生银镜反应。
(6)参照上述合成路线,请填写方框中的空白,以完成制备聚丙烯酸甲酯的合成路线。______
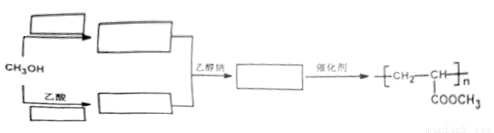
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com