
右图表示外界条件(温度、压强)的变化对下列反应的影响:L(s)+G(g)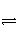
 2R(g) ΔH<0,在图中,Y轴是指( )
2R(g) ΔH<0,在图中,Y轴是指( )

A.平衡混合气体中G的质量分数
B.平衡混合气体中R的质量分数
C.G的转化率
D.L的转化率
科目:高中化学 来源: 题型:
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断不正确的是
A.与NaOH反应的氯气一定为0.15 mol
B.n(Na+)∶n(Cl-) 可能为7∶3
C.若反应中转移的电子为n mol,则n一定大于0.15 mol
D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为7∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于能量转化的认识不正确的是( )
A.绿色植物的光合作用是将光能转变为化学能
B.煤燃烧时化学能转变成热能和光能
C.原电池工作时,化学能转变为电能
D.白炽灯工作时,电能全部转变成光能
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)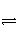
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C生成的速率与C分解的速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g) 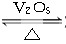 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=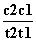
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的SO2和含0.7 mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2
 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
请回答下列问题:
(1)判断该反应达到平衡状态的标志是________(填字母)。
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是________(填字母)。
a.向装置中再充入N2
b.向装置中再充入O2
c.改变反应的催化剂
d.升高温度
(3)求该反应达到平衡时SO2的转化率(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
某些含羟基的药物具有苦味,如下所示结构的氯霉素: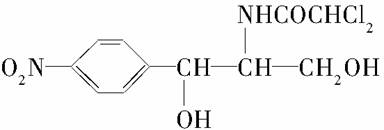 。此药物分子中碳链末端羟基(—OH)中的氢原子换成来自棕榈酸中的原子团
。此药物分子中碳链末端羟基(—OH)中的氢原子换成来自棕榈酸中的原子团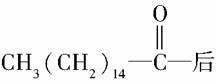 ,苦味消去,成为便于口服的无味氯霉素。以下关于无味氯霉素的叙述中正确的是( )
,苦味消去,成为便于口服的无味氯霉素。以下关于无味氯霉素的叙述中正确的是( )
A.它是棕榈酸的盐类
B.它是棕榈酸的酯类
C.它的水溶性变差,所以苦味消失
D.它的水溶性变良,所以苦味消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com