
下列说法正确的是
A.实验室从海带提取单质碘的方法是:取样灼烧溶解 过滤萃取
B.用乙醇和浓制备乙烯时,可用水浴加热控制反应的温度
C.在室温下,向氯化银的沉淀溶解平衡的体系中加入蒸馏水,氯化银的Ksp保持不变
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
C
【解析】
试题分析:A、实验室从海带提取单质碘的方法是:取样灼烧溶解、过滤得滤液、新制氯水氧化、萃取,错误;B、用乙醇和浓制备乙烯时,温度最好是很快升高到170°C,防止副产物的产生,而水浴加热控制反应的温度太慢,所以应采用直接加热的方式控制温度,错误;D、Ksp是温度常数,只与温度有关,与浓度无关,所以向氯化银的沉淀溶解平衡的体系中加入蒸馏水,氯化银的Ksp保持不变,正确;D、(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,但前者属于蛋白质的盐析,后者属于蛋白质的变性,错误,答案选C。
考点:考查实验室制取碘、乙烯的方法,条件改变对溶度积的影响,蛋白质的盐析与变性的判断


科目:高中化学 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:选择题
将5.4 g Al 投入到200mL 2.0 mol/L的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为
A.HNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液 D.HCl溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高一下学期期中考试化学试卷(解析版) 题型:选择题
下列关于有机物的用途,说法不正确的是
A.甲烷是一种热量高、污染小的清洁能源
B.乙烯最重要的用途是作为植物生长调节剂
C.乙醇是一种很好的溶剂,能溶解多种有机物和无机物
D.酯类物质常用作饮料、糖果、香水、化妆品中的香料
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河西区高三总复习质量检测二理综化学试卷(解析版) 题型:选择题
下表是常温下的五种溶液,下列有关叙述中正确的是( )
| ① | ② | ③ | ④ | ⑤ |
溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | 醋酸钠 |
pH | 11 | 11 | 3 | 3 | 8.3 |
A.表中五种溶液,其中①~④由水电离出的c(H+):②=④>①=③
B.在⑤中加入适量④至溶液呈中性,所得溶液:c(Cl-)>c(Na+)
C.分别将①~④加水稀释至原溶液体积的100倍后溶液的pH:①>②>③>④
D.将①、④两种溶液等体积混合所得溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河北区高三总复习质量检测一理综化学试卷(解析版) 题型:简答题
(15分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素符号是 ;
(2)Z、W形成的气态氢化物的稳定性_______>_______(写化学式)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为___________。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体,该气体能与氯水反应,写出该气体与氯水反应的离子方程式_____________________。
(5)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
A.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
B.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为__________________;
②B的化学式为_________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河北区高三年级总复习质量检测三理综化学试卷(解析版) 题型:填空题
(15分)下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语
回答下列问题:
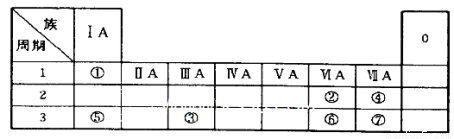
(1)④、⑤、⑦的原子半径由大到小的顺序为_______(用元素符号表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_______>_______。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe+氧化,写出该反应的离子方程式_______。
(4)由表中元素形成的物质可发生如图中的反应,
其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
①写出D溶液与G反应的化学方程式______________.
②写出检验A溶液中溶质的阴离子的方法:______________.
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为_______mol。
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有_______ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河东区高三二模考试理综化学试卷(解析版) 题型:填空题
(14分)如下图装置所示,是用氢氧燃料电池B进行的某电解实验:
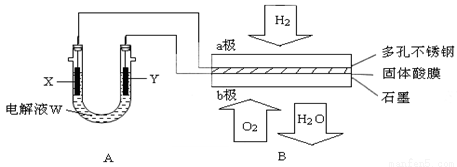
(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH,则下列说法中正确的是________。
A. Li2NH中N的化合价是-1价 B.该反应中H2既是氧化剂又是还原剂
C.Li+ 和H+的离子半径相等 D.此法储氢和钢瓶储氢的原理相同
(2)在电池B工作时:
①若用固体Ca(HSO4)2为电解质传递H+,则电子由________极流出,H+向________极移动。(填“a”或“b”)
②b极上的电极反应式为:________________________________
③外电路中,每转移0.1 mol电子,在a极消耗________上的H2(标准状况下)。
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCI溶液,则B工作时:
①电解池中X极上的电极反应式是 ________________________________。
在X极这边观察到的现象是 _____________________________________。
②检验Y电极上反应产物的方法是 _________________________________。
③若A中其它均不改变,只将电极Y换成铁棒,可实现的实验目的是_____________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河东区高三一模理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片
B.金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻止反应的进一步进行
C.工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质
D.Si、P、S、Cl相应的最高价氧化物对应水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市第二学期期中检测高一化学试卷(解析版) 题型:选择题
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子B.1H与D互称同位素
C.H2O与D2O互称同素异形体D.1H218O与D216O的相对分子质量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com