
| A. | NO2 | B. | NaCl | C. | Na2S | D. | Na2O2 |
分析 A.二氧化氮和水反应生成硝酸显酸性;
B.氯化钠溶于水得到氯化钠溶液,溶液呈中性;
C.硫化钠溶于水,溶液中硫离子水解溶液呈碱性;
D.过氧化钠和水反应生成氢氧化钠显碱性.
解答 解:A.3NO2+H2O=2HNO3+NO,HNO3=H++NO3-,硝酸是酸,电离出氢离子,所以溶液呈酸性,故A错误;
B.氯化钠溶于水得氯化钠溶液,NaCl=Na++Cl-,所以溶液呈中性,故B错误;
C.Na2S溶于水形成的溶液中,硫离子水解,S2-+H2O?HS-+OH-,所以溶液呈碱性,故C正确;
D.过氧化钠(Na2O2)和水反应,2Na2O2+2H2O=4NaOH+O2↑,能生成氢氧化钠,所以溶液呈碱性,故D正确;
故选CD.
点评 本题考查溶液酸碱性的判断,根据溶液中电解质的性质来分析解答即可,题目难度不大.


科目:高中化学 来源: 题型:推断题
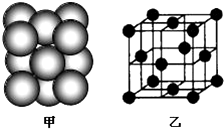
| A元素原子的核外p电子总数比s电子总数少1 |
| B原子核外所有p轨道全满或半满 |
| C元素的主族序数与周期数的差为4 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第十一列 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物的光合作用使得太阳能转化为了化学能 | |
| B. | 燃料燃烧时只是将化学能转化为了热能 | |
| C. | 生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理、有效 | |
| D. | 人类使用照明设备是将电能转化为了光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用排水集气法收集氨气 | |
| B. | 用分液漏斗分离水与乙醇的混合物 | |
| C. | 用淀粉溶液检验溶液中是否存在碘单质 | |
| D. | 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com