
| A、150 mL 1 mol?L-1 NaCl溶液 |
| B、75 mL 2 mol?L-1CaCl2溶液 |
| C、150 mL 2 mol?L-1 KCl溶液 |
| D、75 mL 1 mol?L-1AlCl3溶液 |


科目:高中化学 来源: 题型:
| A、②③ | B、①② |
| C、①②③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中滴加过量氨水:Al3++4OH-═AlO2-+2H2O |
| B、向酸性KMnO4溶液中通入SO2:3SO2+2MnO4-+4OH-=2MnO2↓+3SO42-+2H2O |
| C、澄清石灰水中加足量小苏打溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、醋酸溶液与Cu(OH)2反应:Cu(OH)2+2H+═Cu2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3+H2O=H2SO4 |
| B、Zn+2HCl=ZnCl2+H2↑ |
| C、Fe+CuSO4=FeSO4+Cu |
| D、KCl+AgNO3=KNO3+AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、构成物质的分子中一定含有化学键. |
| B、离子化合物可能含有共价键 |
| C、共价化合物可能含有离子键 |
| D、离子化合物中一定含有金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定管装滴定液时应先用滴定液润洗 |
| B、锥形瓶用作反应容器时一定不能加热 |
| C、蒸馏时温度计水银球可以高于蒸馏瓶支管口 |
| D、振摇分液漏斗时只需要塞上其玻璃塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:
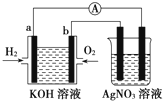 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单质砹易溶于某些有机溶剂 |
| B、AgAt是不溶于水的有色固体 |
| C、HAtO4酸性比HClO4强 |
| D、HAt难溶于水,且受热很难分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
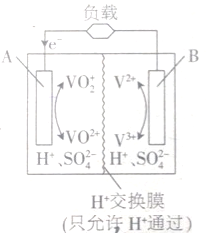 (1)B电极为电池的
(1)B电极为电池的查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com