

分析 (1)铁与水蒸气在加热时反应生成四氧化三铁和氢气;
(2)酒精灯火焰上有铁丝网罩可以使火焰集中,提高加热温度;
(3)本实验生成的气体是氢气,验纯可燃性气体的方法是少量点燃法即爆鸣气法;
(4)棉花中有水,水流到b处,加热可能会使试管炸裂;
(5)遇KSCN溶液不变色,说明溶液中没有铁离子,生成的铁离子被铁还原.
解答 解:(1)铁与水蒸气在加热时反应生成四氧化三铁和氢气,反应方程式为:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,故答案为:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
(2)酒精灯火焰上有铁丝网罩可以使火焰集中,提高加热温度,故答案为:提高酒精灯火焰的温度;
(3)验纯可燃性气体的方法是少量点燃法即爆鸣气法,具体方法是:用向下排空气法(排水法)收集一小试管气体,用拇指扣紧试管口,管口朝下,移向酒精灯火焰,松开拇指,听爆鸣声不尖锐,说明纯净,
故答案为:用向下排空气法(排水法)收集一小试管气体,用拇指扣紧试管口,管口朝下,移向酒精灯火焰,松开拇指,听爆鸣声不尖锐,说明纯净;
(4)试管中有水滴时,加热容易使试管炸裂,可能的原因是加热过程中,棉花中的水流下或水蒸气在试管口处冷凝,故答案为:加热过程中,棉花中的水流下或水蒸气在试管口处冷凝;
(5)铁与水蒸气在加热时反应生成四氧化三铁,用稀硫酸溶解后,加入KSCN溶液没有变红,说明溶液中没有铁离子,可知固体中还有铁,铁离子被铁还原了,所以固体中有Fe3O4和Fe,故答案为:Fe3O4和Fe.
点评 本题考查了铁与水蒸气的反应装置的设计以及反应方程式、生成物的检验,难度不大,注意反应方程式中水是水蒸气.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子间通过共用电子对所形成的化学键叫共价键 | |
| B. | 成键原子间原子轨道重叠越多,共价键越牢固 | |
| C. | 对双原子分子来讲,键能越大,含有该键的分子越稳定 | |
| D. | 键长越长,化学键越牢固 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮及其化合物在化学实验中有广泛应用:
氮及其化合物在化学实验中有广泛应用:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
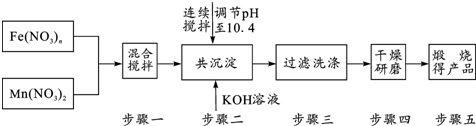
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
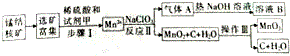
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
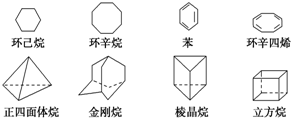 下列是八种环状的烃类物质:
下列是八种环状的烃类物质:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com