
实验一:已知木炭在一定条件下与浓硝酸反应生成两种+4价的氧化物,为了探究一氧化氮(NO)能否与过氧化钠反应,以及反应后的产物中是否有亚硝酸钠(NaNO2),某小组同学设计了如图所示装置(夹持仪器和连接用的胶管已经省略)。

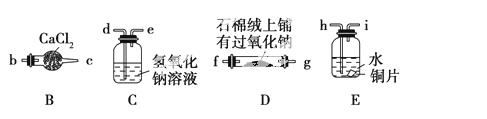
(1)为了完成该实验,虚线框内还需要连接B~E四套装置,按气流方向连接的顺序为:
a→(________) (________)→(________) (________) →(________) (________)→(________) (________) (填仪器接口的字母编号)。连接好仪器,检查气密性,装入药品后,要通入一段时间的氮气,再滴加浓硝酸,点燃酒精灯,通入氮气的主要目的是_____________________ ____________。
(2)装置E中观察到的主要实验现象有____________________________ ____。
(3)装置C的作用是____________________________________________。
(4)某同学经查阅资料后发现亚硝酸是弱酸,性质不稳定,室温下易分解生成一氧化氮。装置D中充分反应后,设计实验证明D中是否有亚硝酸钠生成:______________________________________(写出检验步骤及现象)。
(5)亚硝酸钠在酸性条件下可将I-氧化为I2,同时生成NO,该反应常用于亚硝酸钠含量的测定,请写出该反应的离子方程式:______________________。
实验二:为了证明铜与稀硝酸反应产生一氧化氮,某校同学设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去)。A为注射器,B为两端长短不等的U形管,C是装有NaOH溶液的烧杯,D处是绕成螺旋状的铜丝,K1、K2是止水夹。
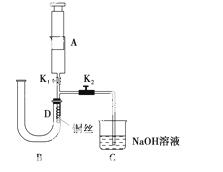
(1)实验时,为在D处收集到NO,以便观察颜色,必须事先在A中吸入一定量的空气。然后________K1(“关闭”或“打开”),打开止水夹K2,从U形管左端注入稀硝酸,当看到______________________时可以确定U形管中空气已被赶尽,关闭止水夹K2。
(2)然后给装置B微微加热,在装置D处产生无色气体,其反应的离子方程式为:
__________________________________________________________。

(3)如何证明D处聚集的是NO而不是H2?
_______________________________________________________。
(4)实验现象观察完毕,关闭止水夹K1,打开止水夹K2,在重力作用下,U形管右端的红棕色混合气体被酸液压入NaOH溶液中吸收,消除了环境污染。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某温度下,向2 L恒容密闭容器中充入1.0 mol A
和1.0 mol B,反应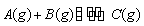 经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A、反应在前5 s的平均速率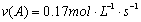
B、保持其他条件不变,升高温度,平衡时 ,则反应的
,则反应的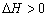
C、相同温度下,起始时向容器中充入2.0 mol C达到平衡时,C的转化率大于80%
D、相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前
查看答案和解析>>
科目:高中化学 来源: 题型:
利用右图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |
|
| A | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要。
完成下列填空:
40.实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
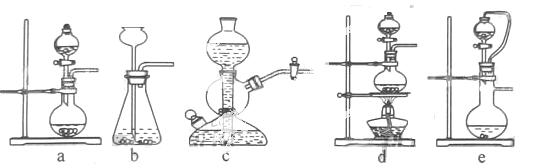
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是 (填写字母)。
41.若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,至少需要称取亚硫酸钠
g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠 g (保留一位小数)。
42.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为SO2+Ca(OH)2→CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O→2CaSO4·2H2O。其流程如下图:
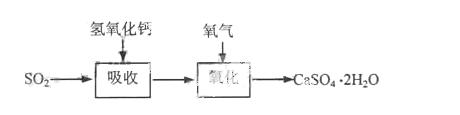
碱法的吸收反应为SO2+2NaOH→Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
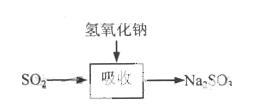
已知:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是 。和碱法相比,石灰-石膏法的优点是 ,缺点是 。
43.在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是( )。
A.NO2通入水中:3NO2+H2O === 2H++2NO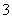 +NO
+NO
B.用两个铜电极电解CuSO4溶液:2Cu2++2H2O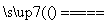 2Cu+O2↑+4H+
2Cu+O2↑+4H+
C.SO2通入FeCl3溶液中:SO2+Fe3++2H2O=== SO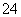 +Fe2++4H+
+Fe2++4H+
D.过量的CO2通入NaAlO2溶液中:2AlO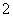 +CO2+3H2O=== 2Al(OH)3↓+CO
+CO2+3H2O=== 2Al(OH)3↓+CO
查看答案和解析>>
科目:高中化学 来源: 题型:
乙烯、苯都是非常重要的有机化工原料。试回答下列问题。
(1)请指出乙烯的一种用途:______________________________________________。
(2)将乙烯通入溴的四氯化碳溶液中,其化学方程式为:__________________。产物的名称是:________。
(3)下列混合物不能用分液漏斗分离的是________。(填选项的符号)
A.四氯化碳和水 B.苯与水
C.酒精与水 D.溴苯与水
(4)写出苯与浓硝酸反应的化学方程式:________________________。
(5)请设计实验证明苯分子中不存在典型的碳碳双键(要求写出操作、现象、结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol乙醇燃烧生成3 mol水
B.1 mol乙醇可以生成1 mol乙醛
C.1 mol乙醇跟足量的金属Na作用得0.5 mol H2
D.乙醇可以制酒精饮料
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,1 mol某气态烃CxHy完全燃烧需要氧气5 mol,则x与y之和可能是( )
A.x+y=5 B.x+y=7
C.x+y=11 D.x+y=13
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com