
【题目】Zn还原SiCl4的反应如下:
SiCl4(g) + 2Zn(l)![]() Si(s) + 2ZnCl2(g) ΔH1
Si(s) + 2ZnCl2(g) ΔH1
SiCl4(g) + 2Zn(g)![]() Si(s) + 2ZnCl2(g) ΔH2
Si(s) + 2ZnCl2(g) ΔH2
下列说法正确的是
A. Zn(l)=Zn(g) ΔH =1/2(ΔH1-ΔH2)
B. 用硅制作的太阳能电池是将化学能转化为电能
C. 增加Zn(g)的量,ΔH2变大
D. 以Zn片、铜片和稀硫酸构成的原电池,Zn片表面有气泡产生。
科目:高中化学 来源: 题型:
【题目】根据如图所示的N2(g)和02(g)反应生成NO(g)过程中的能量变化情况判断,下列说法正确的是
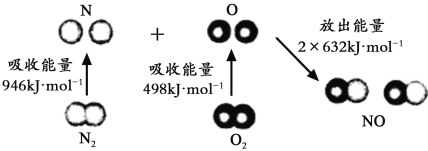
A.N2(g)和O2(g)反应生成NO(g)是放热反应
B.2 mol O原子结合生成O2(g)时需要吸收498 kJ能量
C.1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量
D.2 mol N(g)和2 mol O(g)的总能量为1444 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:
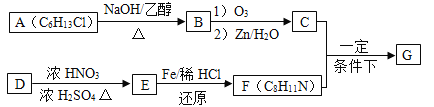
已知以下信息:
①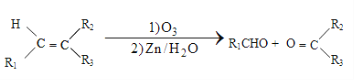
②1molB经上述反应可生成2molC,且C不能发生银镜反应。
③D属于单取代芳香烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤
回答下列问题:
(1)由A生成B的化学方程式为______________,反应类型为________。
(2)D的化学名称是________,由D生成E的化学方程式为:_______________。
(3)G的结构简式为__________________。
(4)F的同分异构体中含有苯环的有多种(不考虑立体异构)。其中核磁共振氢谱中有4组峰,且面积比为6:2:2:1的是____________。(写出其中的一种的结构简式)。
(5)由苯和化合物C经如下步骤可合成N-异丙基苯胺。
![]()
反应条件1所选择的试剂为_______;反应条件2所选择的试剂为________;I的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
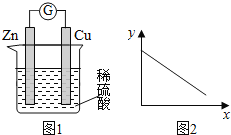
A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:

(1)写出制取乙酸乙酯的化学反应方程式 .
(2)浓硫酸的作用是:① ② .
(3)饱和碳酸钠溶液的主要作用是 .
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 .
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 .
(6)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
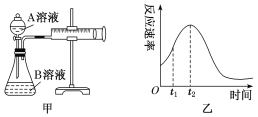
【题目】Ⅰ:用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2 MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
② | 20 mL 0.2 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
(1)该实验探究的是_________________________________因素对化学反应速率的影响。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________ mol·L-1(假设混合溶液的体积为50 mL)。
(3)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:
①产物Mn2+是反应的催化剂,②_______________________________
Ⅱ:当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇,这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)该反应的化学方程式为___________________________________
(2)在恒温恒容密闭容器中,判断上述反应达到平衡状态的依据是________________
a.体系压强不再改变 b.H2的浓度不再改变
c.气体的密度不随时间改变 d.单位时间内消耗H2和CO2的物质的量之比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
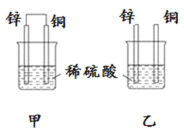
(1)下列说法正确的是____________。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.甲乙两烧杯中溶液的 pH 均增大
(2)同条件下两烧杯中产生同体积的气体,需要的时间甲________乙(填“>”“<”或“=”)。
(3)请写出甲乙图中构成原电池的负极电极反应式:__________________。
(4)当甲中溶液质量增重15.75g时,电极上转移电子数目为______________。
(5)如图为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。写出正极的电极反应方程式为_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A~E是中学化学常用的五种仪器:

回答下列问题:
(1)上述仪器中,使用时需首先检查是否漏水的有_________(填标号)。
(2)下列实验操作中,使用到仪器C的是________(填标号)。
a.分离水和酒精的混合物
b.分离水和四氯化碳的混合物
c.分离水和泥砂的混合物
d.提纯Fe(OH)3胶体
(3)某化学兴趣小组实验过程中,需要480 mL0.5mol·L-1 NaOH溶液。
①除上述提供的仪器外,还用到的玻璃仪器有_________________。
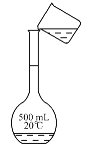
②如图所示,转移操作中的一处错误是_____________________。
③在配制过程中,下列情况会导致所配溶液浓度偏低的是_______(填标号)。
a.准确称量9.6gNaOH
b.溶解时未冷却至室温就转移
c.在定容时,仰视刻度线
d.加水至刻度线后摇匀,发现液面低于刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
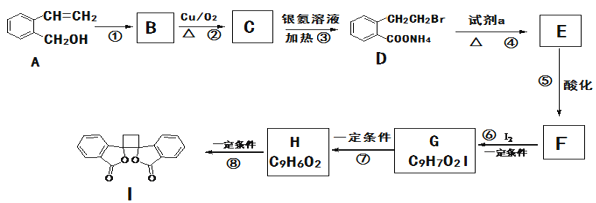
【题目】具有抗菌作用的白头翁素衍生物I的合成路线如图所示:
已知:
ⅰ.R-HC=CH-R’+R”COOH![]()
ⅱ.R-HC=CH-R”![]() (以上R、R’、R”代表氢、烷基或芳基等)。
(以上R、R’、R”代表氢、烷基或芳基等)。
回答下列问题:
(1)反应①的反应类型是___。
(2)写出反应②的化学方程式是___。
(3)合成过程中设计步骤①和④的目的是___。
(4)试剂a是___。
(5)下列说法正确的是___(选填字母序号)。
a.物质A极易溶于水 b.③反应后的试管可以用硝酸洗涤
c.F生成G的反应类型是取代反应 d.物质D既能与盐酸反应又能与氢氧化钠钠溶液反应
(6)由F与I2在一定条件下反应生成G的化学方程式是___;此反应同时生成另外一个有机副产物且与G互为同分异构体,此有机副产物的结构简式是___。
(7)已知:RCH2Br![]() R-CH=CH-R1
R-CH=CH-R1
以乙烯起始原料,结合已知信息选用必要的无机试剂合成 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___。
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com