
【题目】需要配制500 mL 0.5 mol·L-1氢氧化钠溶液,经测定实际所配氢氧化钠溶液的浓度为0.45 mol·L-1。可能的原因是( )
A. 转移时溶液没有冷却至室温 B. 容量瓶没有烘干
C. 称量氢氧化钠固体时砝码放反了 D. 定容时仰视读数
【答案】D
【解析】
0.45mol/L<0.5mol/L,即操作失误使所配溶液浓度偏小;根据公式cB=![]() 分析,操作失误使nB偏大或V(aq)偏小,会使所配溶液浓度偏大,反之偏小。
分析,操作失误使nB偏大或V(aq)偏小,会使所配溶液浓度偏大,反之偏小。
0.45mol/L<0.5mol/L,即操作失误使所配溶液浓度偏小;
A项,NaOH溶于水放热,转移时溶液没有冷却至室温,根据“热胀冷缩”原理,冷却后溶液体积偏小,所配溶液浓度偏大,不符合题意;
B项,容量瓶没有烘干,对所配溶液浓度无影响,不符合题意;
C项,配制500mL0.5mol/LNaOH溶液需要称量NaOH固体的质量为m(NaOH)=0.5mol/L×0.5L×40g/mol=10.0g,称量时不需要使用游码,称量NaOH固体时砝码放反了对所配溶液的浓度无影响,不符合题意;
D项,定容时仰视读数,所配溶液体积偏大,所配溶液浓度偏小,符合题意;
答案选D。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。
(1)乙醇、乙酸和浓硫酸的加入顺序是___________。制取乙酸乙酯的反应原理为:__________________________________。

(2)为证明浓硫酸在该反应中起到了______和________的作用, 为证明其作用,某同学利用上图所示装置进行了以下四个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
实验编 号 | 试管I中的试剂 | 试管II中的试剂 | 测得有机层的厚度/cm |
A | 2mL乙醇、2mL乙酸、1mL18mo/L浓硫酸 | 5.0 | |
B | 3mL乙醇、2mL乙酸 | 饱和碳酸钠溶液 | 0.1 |
C | 3mL乙醇、2mL乙酸、6mL3mol/L硫酸 | 1.2 | |
D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
①验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_____mL和_____mol/L。
②分析实验_______(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是___________。
(3)饱和碳酸钠溶液的作用是溶解没有反应的乙醇,除去没有反应的乙酸和___________,本实验装置有明显的缺陷,其可能造成的后果是__________________________。
(4)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,一个可能的原因是_______________。
(5)分离饱和碳酸钠溶液和乙酸乙酯的方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.镍镉电池、锂电池和锌锰电池都是二次电池
B.燃料电池是一种高效但是会污染环境的新型电池
C.化学电池的反应原理是氧化还原反应
D.铅蓄电池放电时正极是Pb,负极是PbO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用实验室制得的乙烯(C2H5OH![]() CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是
CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是

A. 装置①和装置③中都盛有水,其作用相同
B. 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C. 产物可用分液的方法进行分离,1,2﹣二溴乙烷应从分液漏斗的上口倒出
D. 制备乙烯和生成1,2﹣二溴乙烷的反应类型分别是消去反应和加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列与氯气有关的问题。
(1)氯气溶于水中,所得溶液具有漂白性是因为含有(写化学式)______________,有关反应的化学方程式是_________________________________________。
(2)标准状况下,a L氢气在过量的b L氯气中燃烧,所得混合物用100mL3.00mol/L的NaOH溶液恰好完全吸收,上述过程发生的有关化学反应方程式除HCl+NaOH=NaCl+H2O外,还有___________________,________________。氯气的体积b=______。
(3)下列化学反应的实验现象描述错误的是____________________。
A.钠在氯气中燃烧发出黄色火焰,有大量白雾
B.红热的铜丝在氯气中燃烧,生成蓝色固体CuCl2
C.铁丝在氯气中燃烧产生棕色的烟,溶于水其水溶液呈黄色
D.氢气在氯气中燃烧产生苍白色火焰,有大量白雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图给出了8种有机化合物的转化关系,请回答下列问题:
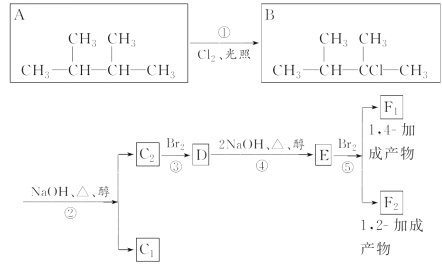
(1)根据系统命名法,化合物A的名称是________。
(2)上述框图中,①是________反应,③是________反应。(填反应类型)
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:___________________。
(4)C2的结构简式是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物会形成光化学烟雾和酸雨,可采取下列方法对氰氧化物进行处理。
(1) SNCR脱硝技术的原理:
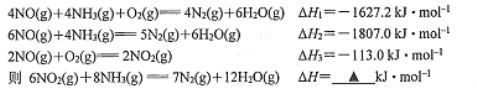 ____________
____________
(2) NSR (NOx储存还原)工作原理:
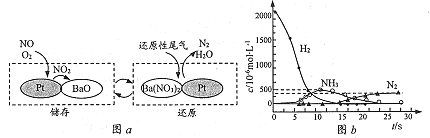
NOx的储存和还原在不同时段交替进行,如图a所示。
①NOx储存转化为Ba(NO3)2过程中,参加反应的NO和02的物质的量之比为_________________。
②H2还原Ba(NO3)2的过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为__________________。
(3)SCR消除氮氧化物的反应原理:![]()
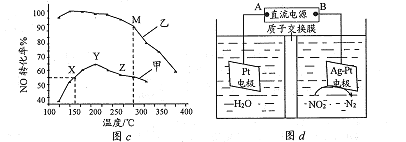
其他条件相同,某密闭容器中分别投入NH3、NO、O2,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图c所示。在催化剂甲作用下,图中Y点处(对应温度为210℃)NO的转化率一定不是该温度下的平衡转化率的原因是__________________。工业实际选择催化剂乙的原因是___________________。
(4)①用石灰乳吸收氨的氧化物,原理为:
![]()
为使吸收充分![]() ___(选填“≥”或“≤”)l。
___(选填“≥”或“≤”)l。
②目前可采用电解的方法除去废水中的NO2-,原理如图d所示。写出阴极的电极反应式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如下图所示,不正确的是( )
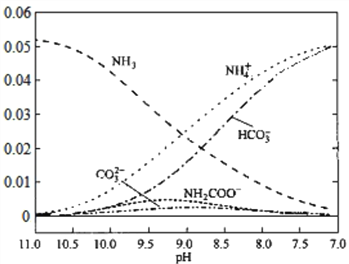
A. 在pH=9.0时,c(NH4+)>c(HCO3ˉ)>c(NH2COOˉ)>c(CO32-)
B. 在氨-水体系中不断通入CO2,体系中始终存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3ˉ)+c(OHˉ)
C. 随着CO2的通入,![]() 不断减小
不断减小
D. pH=7时,水的电离程度最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com