
【题目】国际奥委会公布的违禁药物有138种,其中某种兴奋剂分子结构如图,关于它的说法正确的是( )

A. 该物质属于芳香烃
B. 该分子中所有碳原子共面
C. 1mol该物质与氢氧化钠溶液完全反应,最多消耗2molNaOH
D. 该物质的化学式为C15H24ClNO2
科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入500 mL某氢氧化钠溶液中,充分反应后将溶液在低温下蒸发,得到不含结晶水的白色固体A,取三份质量不相同的A试样分别与50mL相同浓度的盐酸溶液反应,得到标准状况下气体体积与固体A的质量关系如表所示:
组别 | ① | ② | ③ |
A的质量 | 3.80 | 5.70 | 7.60 |
气体体积(mL) | 896 | 1344 | 1120 |
(1)试判断:A的成分___。
(2)盐酸物质的量浓度为___molL﹣1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
A.分离酒精和水![]()
B.分离胶体和溶液
C.除去碳酸钠固体中的碳酸氢钠
D.比较碳酸钠和碳酸氢钠的稳定性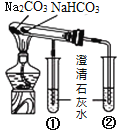
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某同学进行CO2与Na2O2反应的探究实验,回答下列问题。
(1)用如图装置制备纯净的CO2
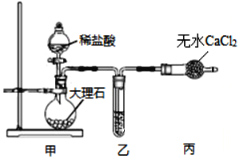
①甲装置中盛放稀盐酸的仪器名称是_____,乙装置中应加入的试剂是_______________。
②装置甲中反应的离子方程式为__________。
(2)按照下面的装置图进行实验(夹持装置略)。
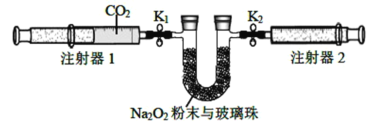
①先组装仪器,然后_______________,再用注射器1抽取100 mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1的活塞,可观察到的现象是_______________。
③实验过程中,需缓慢推入CO2,其目的是________________,反应的化学方程式为_______________。
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体体积为65 mL,则反应消耗CO2的体积是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中X2 (g)+2Y2 (g)![]() Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
A.c(Z) ═0.45mol/LB.c(X2) ═0.3mol/L
C.c(X2) ═0.5mol/LD.c(Y2) ═0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下分别测得反应2SO2+O2![]() 2SO3的化学反应速率,其中表示该反应进行得最快的是( )
2SO3的化学反应速率,其中表示该反应进行得最快的是( )
A.v(SO2)=4mol/(L·min)B.v(O2)=3mol/(L·min)
C.v(SO2)=0.1mol/(L·s)D.v(O2)=0.1mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
选项 | 化学性质 | 实际应用 |
A |
| 泡沫灭火器灭火 |
B |
| 可作面包的发泡剂 |
C | 乙酸具有酸性 | 常用于工业管道去除水垢 |
D | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
A.AB.B.C.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中根据![]() 已知
已知![]() 熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备
熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备![]() 固体。
固体。
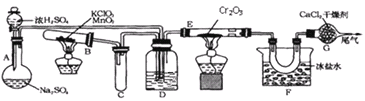
(1)实验开始时,先点燃的酒精灯是_________(填编号)。
(2)装置D中浓硫酸的作用除了混合气体并观察气体流速外还有___________。
(3)装置F的作用是____________________。
(4)由于可逆反应,所以从E管出来的气体中含有![]() 、
、![]() 。为了证明含有
。为了证明含有![]() 可以将该气体通入________(填下列编号,下同)、证明含有
可以将该气体通入________(填下列编号,下同)、证明含有![]() 可以将该气体通入_____________。
可以将该气体通入_____________。
A.品红 B.溴水 C.![]() 溶液 D.
溶液 D.![]() 溶液
溶液
(5)如果没有装置G,则F中可能看到_________________。
(6)从装置G导出的尾气常可以用烧碱或石灰乳吸收。请写出用足量烧碱吸收尾气的离子方程式为:_________________________________________________________。
(7)尾气常采用烧碱或石灰乳吸收,请分析比较两种吸收剂吸收的优点__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空:
(一)下列 8 组物质或粒子:
①14N 和 14C ②16O 和 18O ③氰酸铵(NH4CNO)与尿素[CO(NH2)2] ④足球烯(C60)和金刚石 ⑤CH3CH2CH2CH3 和 CH(CH3)3 ⑥CH3CH2CH3 和 CH3(CH2)2CH3 ⑦ ![]() 和
和 ![]() ⑧
⑧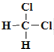 和
和![]()
(1)互为同素异形体的是__________(填编号,下同);
(2)互为同位素的是________________;
(3)互为同系物的是___________;
(4)互为同分异构体的是________________。
(二)有下列几种晶体:
A、水晶 B、冰醋酸 C、白磷 D、金刚石 E、晶体氩 F、干冰 G、氟化钠 H、过氧化钠
(1)属于原子晶体的化合物是__________________(填序号,下同);
(2)含有共价键的离子晶体是________________________;
(3)受热融化时需要克服共价键的晶体是_________________________;
(4)写出下列物质的电子式:过氧化钠_____________,二氧化碳________________。
(三)某烷烃的结构简式为:
(1)用系统命名法命名该烃:__________________________;
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构可能有 ________种(不包括立体异构,下同);
(3)若该烷烃是由炔烃加氢得到的,则原快烃的结构有_________________种;
(4)该烷烃在光照条件下与氯气反应,生成的一氧代烷最多有____________种。
(四)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。 当把 0.4mol 液态肼和0.8mol H2O2 混合反应,生成氮气和水蒸气,放出 256.7KJ 的热量(相当于 25℃、101 kPa 下测得的热量)。
①反应的热化学方程式为________________________________;
②已知 H2O(1)=H2O(g) ΔH=+44kJ/mol。
则 16g 液态肼与液态双氧水反应生成液态水时放出的热量是_________________kJ;
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com