
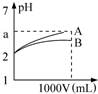
 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )| A、①② | B、③④ | C、①③ | D、②④ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| 1 |
| 2 |
| 1 |
| 2 |
| 温度/Kn(H2)/n(CO2)CO2转化率/% | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ |
| B、在pH=2的溶液中:ClO-、SO32-、Na+、K+ |
| C、含有CO32-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+ |
| D、能与铝粉反应生成氢气的溶液中:Na+、Al3+、CH3COOO-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、实验室制备氢氧化铁胶体:Fe3++3H2O
| ||||
| B、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | ||||
| C、碳酸氢铵溶液中加入过量的氢氧化钠溶液:NH4++HCO3-+2OH-=NH3?H2O+CO32-+H2O | ||||
| D、氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、27 mg |
| B、54 mg |
| C、106 mg |
| D、216 mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用100ml 4mol/L盐酸与8.7gMnO2共热能制取氯气0.2NA |
| B、一定温度下0.1L 0.1mol/L的HA和1L0.01mol/L的HA所含A-微粒数均为0.01NA |
| C、4.5 gSiO2晶体中含有的硅氧键数目为0.3 NA |
| D、标准状况下3.36 L CCl4含碳原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com