
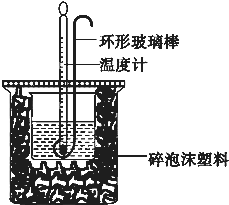
 ��ѧ��Ӧ�е���ЧӦ
��ѧ��Ӧ�е���ЧӦ| ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
| ���� | NaOH��Һ | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1.4212KJ��1mol |
| 0.025mol |


 �żӾ���ϵ�д�
�żӾ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������N��PԪ�ص�������ˮ����ֱ���������ũ�� |
| B�����ۡ���ά�ء������ʡ������Ƕ�����Ȼ�߷��ӻ����� |
| C�����ع��͡���Ȼ�������к������ԡ��ع��͡����з�����Ƶ����͡�ú�ͣ��ﵽ���Ϊ����Ŀ�� |
| D�������ʡ���֬�����Ƕ���ˮ�⣬��ˮ����ﶼ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4+��NO3-��SiO32-��Na+ |
| B��Na+��Ba2+��HCO3-��AlO2- |
| C��NO3-��Mg2+��K+��Cl- |
| D��NO3-��K+��AlO2-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CaO+H2O�TCa��OH��2 | ||||
| B��2Na2O2+2H2O�T4NaOH+O2�� | ||||
| C��2Na+2H2O�T2NaOH+H2�� | ||||
D��C+H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 | B��3 | C��4 | D��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��C3H7Cl |
| B��C4H10 |
| C��C5H12 |
| D��CH2Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ͨ�����ʯ��ˮ�����Ư�� |
| B����ú���и���ý�̿��ú���͵Ȼ���ԭ�� |
| C����ʯ�ͷ������ϩ����ϩ��1��3-����ϩ |
| D����Ũ����Ͷ������̼��ȷ�Ӧ�Ʊ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
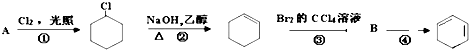
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
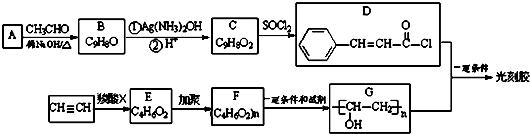
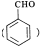
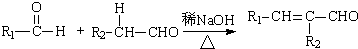 ��R��R��Ϊ�������⣩
��R��R��Ϊ�������⣩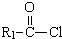 +R2OH
+R2OH| һ������ |
 +HCl��R��R��������
+HCl��R��R��Ϊ������| NaOH��Һ |
| �� |
| CH3COOH |
| Ũ���ᣮ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com