
| A、降低温度 |
| B、增大压强 |
| C、增大CO的浓度 |
| D、使用催化剂 |
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
| 物质 | CO | H2 | CH3OH |
| 物质的量/(mol) | 0.4 | 0.4 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
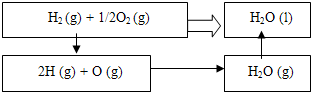
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图把混合气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( )
如图把混合气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( )| 选项 | 气体 | A中试剂 | B中试剂 |
| A | SO2、CO2 | 酸性KMnO4溶液 | 品红溶液 |
| B | Cl2、HCl | 浓硫酸 | KI淀粉溶液 |
| C | NH3、CO2 | 浓硫酸 | 酚酞试液 |
| D | HCl、CO2 | NaHCO3饱和溶液 | 澄清石灰水 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、碳原子中的质子数为6 |
| B、碳的相对原子质量是12.01g |
| C、碳属于金属元素 |
| D、碳的氧化物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
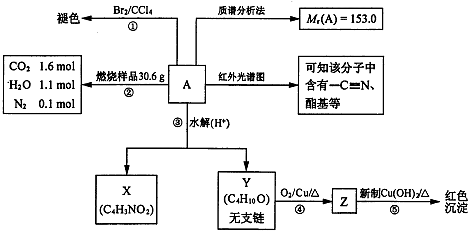
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、探究Na在空气中放置后的生成物是Na2CO3 |
| B、探究Na与水反应有O2生成 |
| C、探究含铁元素的营养酱油中的铁以Fe2+或Fe3+的形式存在 |
| D、探究向滴有酚酞的NaOH溶液中通Cl2时,溶液褪色是NaClO的漂白性所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgCl>AgI>Ag2CrO4 |
| B、AgCl>Ag2CrO4>AgI |
| C、Ag2CrO4>AgI>AgCl |
| D、Ag2CrO4>AgCl>AgI |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com