
| ||
| ||
| B |
| A |
| B |
| A |
| ||
| ||
| B |
| A |
| B |
| A |


科目:高中化学 来源: 题型:058
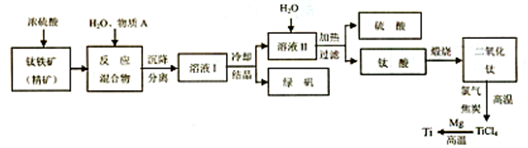
中国西部地区自然资源丰富,在矿产资源中,钛、铜、汞、铅、锌等30多种矿产储量居全国第一,攀枝花的矾钛铁矿、云南的锡矿等在全国都占十分重要的地位.
(1)矾钛铁矿的主要成分可用化学式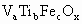 来表示,其中V显正+5价,Ti显+4价,Fe显+价,则x的值是_______(用含a、b、c的代数式表示).
来表示,其中V显正+5价,Ti显+4价,Fe显+价,则x的值是_______(用含a、b、c的代数式表示).
(2)经分离矾钛铁矿石最终可得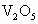 、
、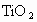 等物质,试写出
等物质,试写出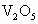 ,跟Al粉反应的化学方程式_____________.
,跟Al粉反应的化学方程式_____________.
(3)已知 .某学生兴趣小组设计一套实验装置利用上述反应以制得
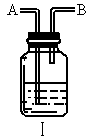
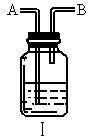
.某学生兴趣小组设计一套实验装置利用上述反应以制得 ,装置中尾气处理部分如图Ⅰ所示,瓶中应加入_____________溶液,在导管口B处应______________.
,装置中尾气处理部分如图Ⅰ所示,瓶中应加入_____________溶液,在导管口B处应______________.
(4)装置图Ⅱ可用于收集下列气体中的_________________(填字母).
|
A.CO |
B.HCl |
C. |
|
D. |
E. |
F. |

查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
中国西部地区自然资源丰富,在矿产资源中,钛、铜、汞、铅、锌等30多种矿产储量居全国第一,攀枝花的矾钛铁矿、云南的锡矿等在全国都占十分重要的地位.
(1)矾钛铁矿的主要成分可用化学式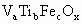 来表示,其中V显正+5价,Ti显+4价,Fe显+价,则x的值是_______(用含a、b、c的代数式表示).
来表示,其中V显正+5价,Ti显+4价,Fe显+价,则x的值是_______(用含a、b、c的代数式表示).
(2)经分离矾钛铁矿石最终可得 、
、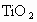 等物质,试写出
等物质,试写出 ,跟Al粉反应的化学方程式_____________.
,跟Al粉反应的化学方程式_____________.
(3)已知 .某学生兴趣小组设计一套实验装置利用上述反应以制得
.某学生兴趣小组设计一套实验装置利用上述反应以制得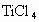 ,装置中尾气处理部分如图Ⅰ所示,瓶中应加入_____________溶液,在导管口B处应______________.
,装置中尾气处理部分如图Ⅰ所示,瓶中应加入_____________溶液,在导管口B处应______________.
(4)装置图Ⅱ可用于收集下列气体中的_________________(填字母).
|
A.CO |
B.HCl |
C. |
|
D. |
E. |
F. |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com