
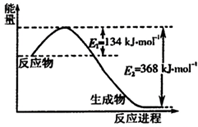
 ����һ�ֵ����Ϻ����ḻ��Ԫ�أ������仯������о���������������������Ҫ���壮
����һ�ֵ����Ϻ����ḻ��Ԫ�أ������仯������о���������������������Ҫ���壮

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д� ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
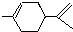 �������й������Ʋⲻ��ȷ���ǣ�������
�������й������Ʋⲻ��ȷ���ǣ�������| A������ʽΪC10H16 |
| B��������ΪҺ̬��������ˮ |
| C�����ڷ����� |
| D��1mol��������1molHCl�ӳ����ò��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HA��ǿ | B��HB��ǿ |
| C������һ�� | D�����Ƚ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ʹ������Ȼ�̼��Һ��ɫ��˵����������û������ϩ���������Ƶ�̼̼˫�� |
| B������ˮ���ɼ��𱽷���Һ��2��4-�Ѷ�ϩ�ͼױ� |
| C�������������£�CH3CO18OC2H5��ˮ�������CH3CO18OH��C2H5OH |
| D������ʽΪC4H10O����������Ʒ�Ӧ�ų��������л���������4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
C��
| ||
| D����1��10-14-5��10-5�� mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1.0��10-7mol?L-1 |
| B��1.0��10-6mol?L-1 |
| C��1.0��10-12mol?L-1 |
| D��1.0��10-14mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʵ��������240mL2.0mol/L��NaOH��Һ��Ӧ��NaOH����19.2g |
| B��Ϊ��ֹҩƷ��Ⱦ����ʣ�Ľ����Ʒ�������Ͱ�� |
| C����25 mL��Ͳ��ȡ22.6 mL���� |
| D����������ƽ��ȡ8.75 gʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Sn2+��Fe2+��Ge3+ |
| B��Sn2+��Ge3+��Fe2+ |
| C��Ge3+��Fe2+��Sn2+ |
| D��Fe2+��Sn2+��Ge3+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com