
| A. | 2SO2+O2?2SO3 △H=-196.6kJ/mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═2H2O(l)△H=-285.8kJ/mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6kJ•mol-1 | |
| D. | C(s)+O2(g)═CO2(g)△H=+395.9kJ/mol-1 |
分析 A.没有标出物质的聚集状态;
B.H2与O2的化合反应为放热反应;
C.氢气燃烧为放热反应;
D.碳燃烧放热反应.
解答 解:A.没有标出物质的聚集状态,正确的写法为2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol,故A错误;
B.H2与O2的化合反应为放热反应,符合热化学方程式的书写要求,故B正确;
C.氢气和氧气反应是放热反应,2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1,故C错误;
D.C的燃烧为放热反应,正确的写法为C(s)+O2(g)═CO2(g);△H=-393.5kJ/mol,故D错误;
故选B
点评 本题考查热化学方程式的书写,题目难度不大,注意热化学方程式的书写注意事项.


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{53}^{127}$I和${\;}_{53}^{131}$I的核外电子数不同 | |
| B. | ${\;}_{53}^{127}$I和${\;}_{53}^{131}$I的中子数分别为74和78 | |
| C. | ${\;}_{53}^{127}$I和${\;}_{53}^{131}$I属不同种元素 | |
| D. | ${\;}_{53}^{127}$I和${\;}_{53}^{131}$I是同一种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| C. | 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 缩小容器的体积使压强增大 | B. | 体积不变,充入N2 | ||
| C. | 恒容,充入He | D. | 降低反应温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
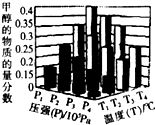 反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,
反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,| A. | P3>P2,T3>T2 | B. | P2>P4,T4>T2 | C. | P1>P3,T1>T3 | D. | P1>P4 T2<T3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
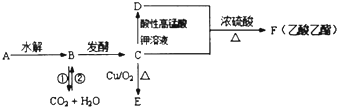
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入BaCl2溶液中至饱和,无沉淀产生,再通入过量NH3,产生沉淀 | |
| B. | 高纯硅常用作光导纤维的原料 | |
| C. | 用AlCl3溶液制取Al(OH)3,沉淀剂选用氨水比选用NaOH溶液好 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,反应速率加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com